Wichtige Gittertypen sind das kubisch-flächenzentrierte (kfz), das kubisch-raumzentrierte (krz) und das hexagonal dichtest-gepackte Gitter (hdp).
Einleitung
Im Abschnitt Gitterstruktur von Metallen wurde erläutert weshalb sich die Atome in einem Metall in einer bestimmten Regelmäßigkeit anordnen und so eine Gitterstruktur ausbilden. Nur in seltenen Fällen entsteht dabei ein einfaches kubisches Gitter, wie es in der unteren Animation zu sehen ist.
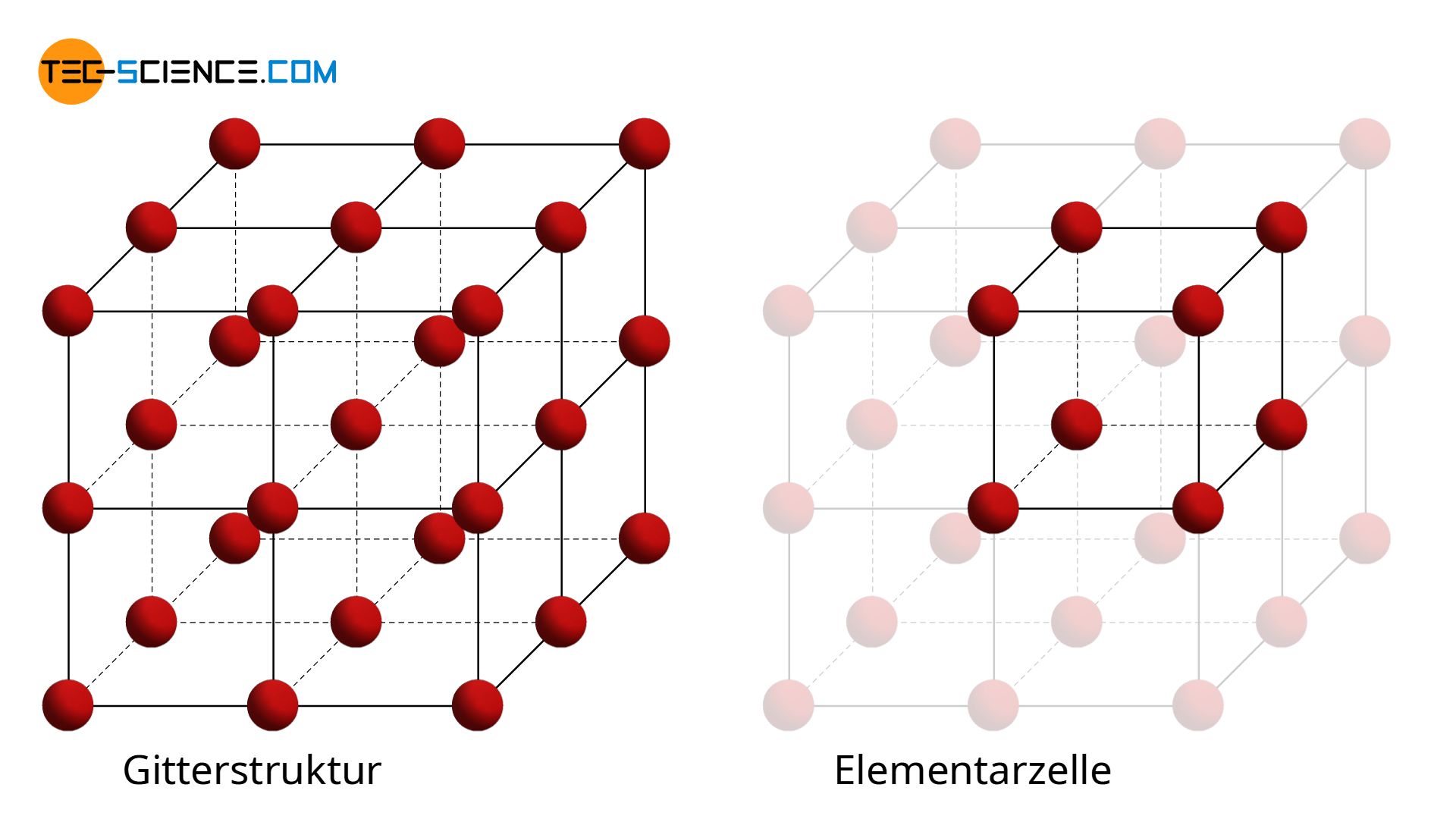
Von wesentlich größerer technischer Bedeutung sind Abwandlungen von dieser Gitterstruktur. Hierzu zählen das kubisch-raumzentrierte Gitter (krz) und das kubisch-flächenzentrierte Gitter (kfz), sowie das hexagonale Gitter (hdp).
Der Unterschied in der Gitterstruktur hat insbesondere starke Auswirkungen auf die Verformbarkeit der entsprechenden Metalle! Während das kfz-Gitter die größte und das hdp-Gitter die geringste Verformbarkeit zeigt, besitzt das krz-Gitter eine Verformbarkeit die zwischen den anderen Gitterstrukturen liegt.
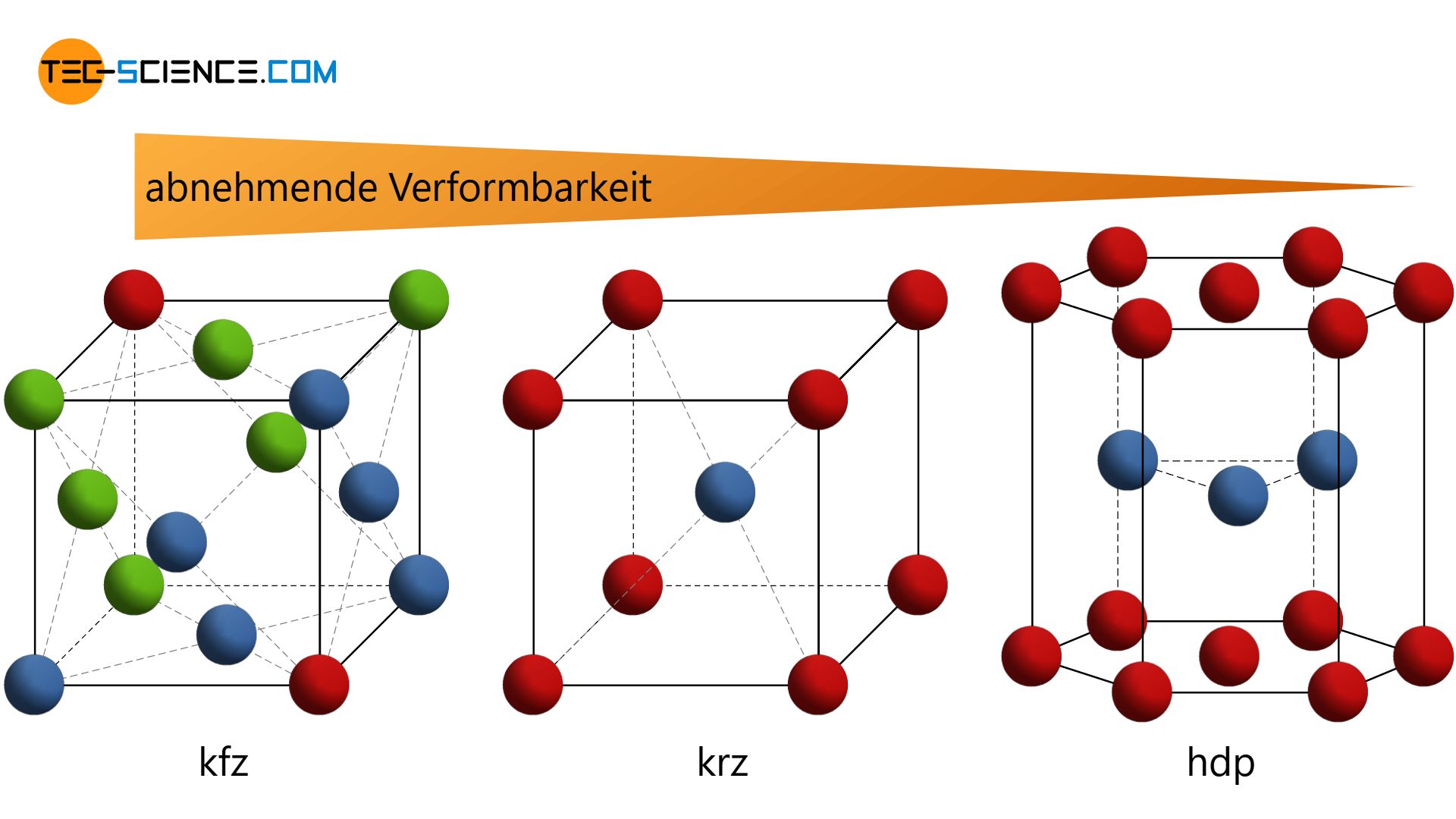
Um diese Unterschiede in der Verformbarkeit nachvollziehen zu können, muss zunächst der Aufbau der unterschiedlichen Gittertypen verstanden werden. Aus diesem Grund wird in diesem Beitrag auf das Zustandekommen der drei wichtigsten Gittertypen näher eingegangen.
Kubisch-raumzentriertes Gitter
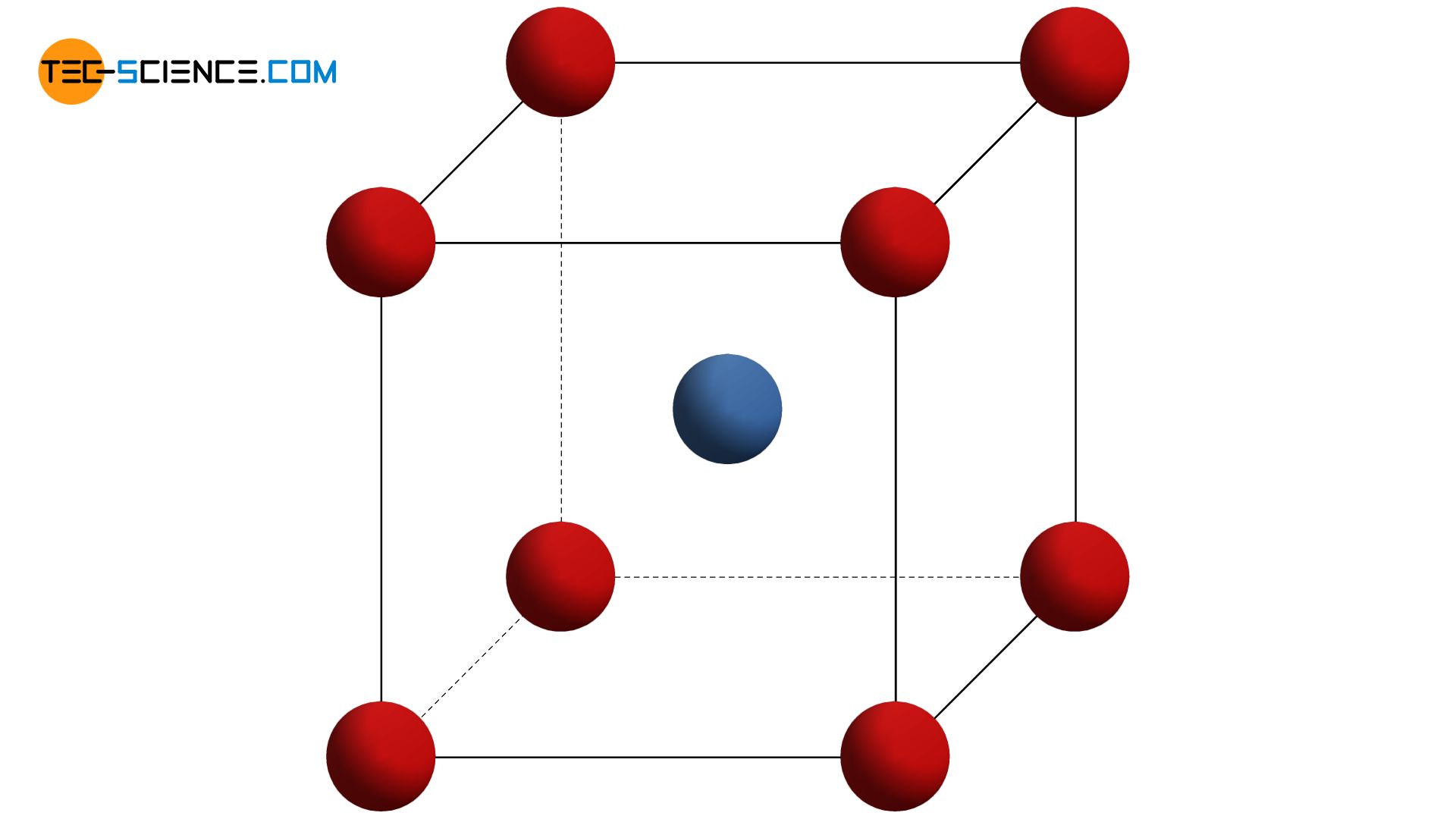
Eine Abwandlung des kubisch-primitiven Gitters ist das sogenannte kubisch-raumzentrierte Gitter (krz). In dieser Gitterstruktur liegen die einzelnen Atomebenen in den Lücken der jeweils darunter liegenden Ebene. Wie beim kubisch-primitiven Gitter hat auch dabei die Elementarzelle die Grundform eines Würfels (Kubus). Zusätzlich zu den Eckatomen, die jeweils in den Ecken der würfelförmigen Elementarzelle sitzen, befindet sich nun ein weiteres Atom zentriert in der Raummitte. Diese Atombelegung der Elementarzelle ist Namensgeber des kubisch-raumzentrierten Gitters.
Im kubisch-raumzentrierten Gitter (krz) befindet sich neben den Eckatomen ein weiteres Atom in der Mitte der würfelförmigen Elementarzelle!
Typische Vertreter solcher kubisch-raumzentrierten Strukturen sind unter anderem die Metalle Eisen, Chrom, Molybdän, Vanadium und Wolfram.
Im kubisch-raumzentrierten Gitter steht ein Atom in unmittelbarem Kontakt zu acht umgebenden Atome. Man bezeichnet diese Anzahl an direkten Nachbaratomen auch als Koordinationszahl. Die Koordinationszahl im krz-Gitter beträgt folglich 8. Im einfachen kubischen Gitter kommt man hingegen auf eine Koordinationszahl von 6.
Die Koordinationszahl beschreibt die Anzahl an direkt benachbarten Atomen!
Für die Darstellung von Elementarzellen ist es sinnvoll die Atome verkleinert zu zeichnen, auch wenn sich diese in Wirklichkeit „berühren“. Um die räumliche Anordnung der Atome zu verdeutlichen, ist es ferner üblich die Grundform der Elementarzelle durch Striche anzudeuten. Diese Striche stellen keine Bindungskräfte dar!
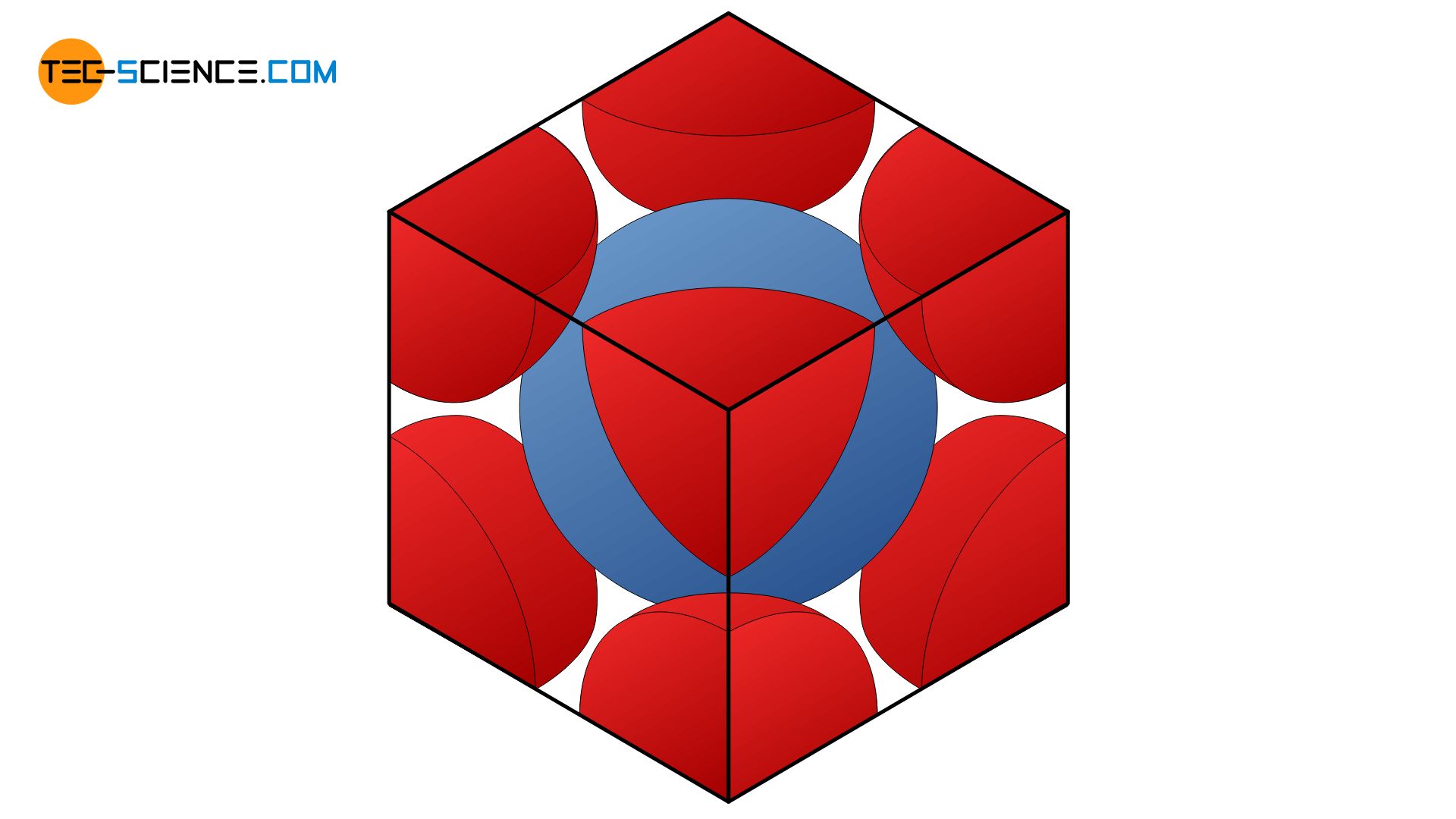
Werden die Atome realistischer Weise als sich berührende Kugeln betrachtet, so kann auf diese Weise die sogenannte Packungsdichte eines Gitters ermittelt werden. Diese gibt an, wie viel Prozent der Elementarzelle mit Atome ausgefüllt ist. Für das kubisch-raumzentrierte Gitter lässt sich auf diese Weise eine Packungsdichte von 0,68 ermitteln. Dies bedeutet, dass 68 % des gesamten Gittervolumens (bzw. der Elementarzelle) mit Atomen besetzt sind. Die restlichen 32 % entfallen auf die „Lücken“ zwischen den Atomen. Die Herleitung dieser Packungsdichte wird in einem eigenen Beitrag gezeigt.
Als Packungsdichte bezeichnet man das Verhältnis des Atomvolumens zum Gesamtvolumen der Elementarzelle!
Hexagonal-dichtestgepacktes Gitter
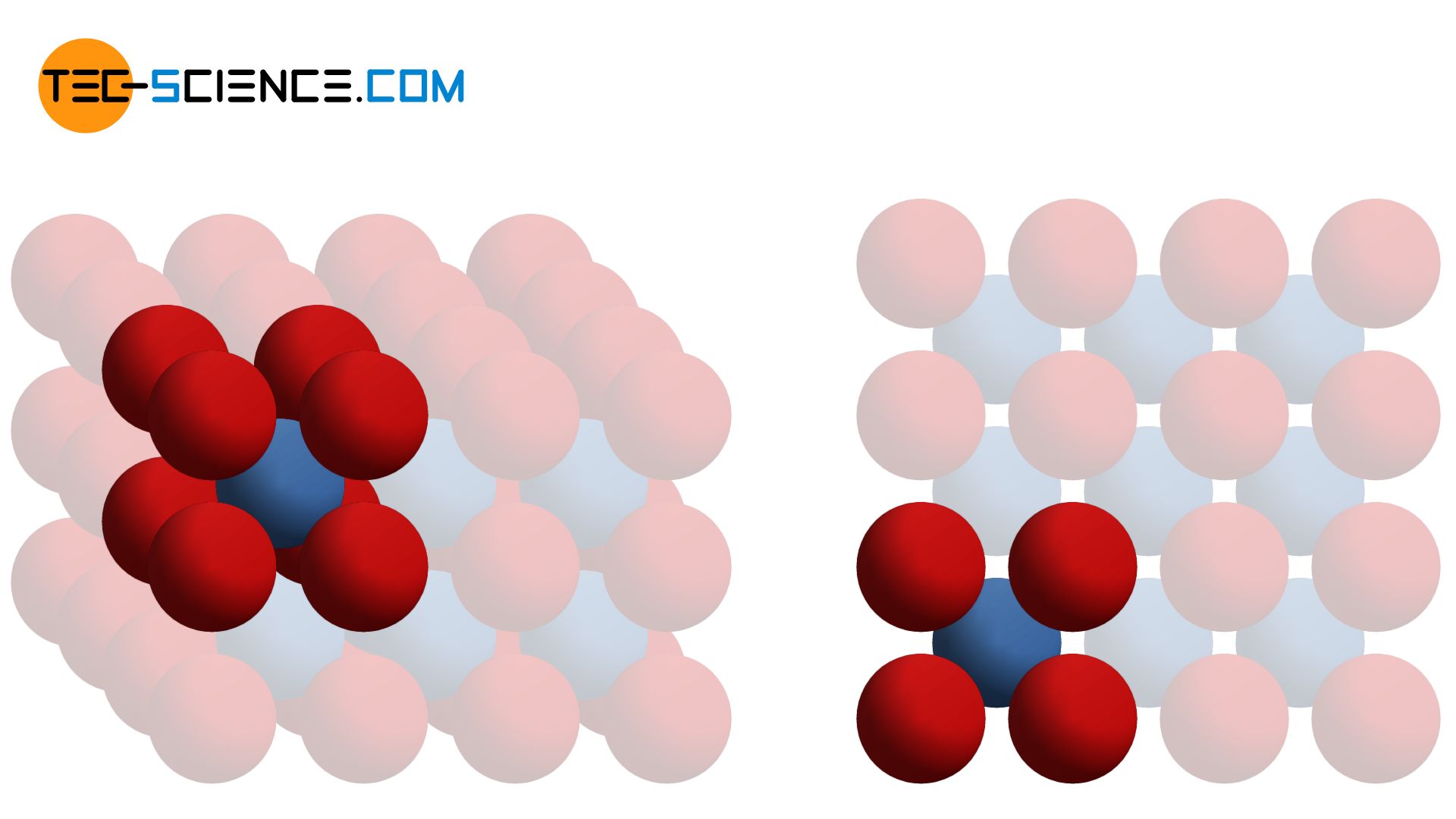
Im kubisch-raumzentrierten Gitter weisen die übereinander liegenden Atomebenen Lücken auf, sodass die jeweils darunter liegende Atomebene genau in die Lücken der oberen passt. Die Atomebenen sind somit nicht maximal gepackt. Anders sieht dies beim hexagonalen Gitter aus.
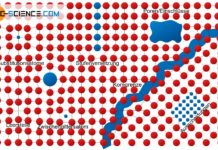
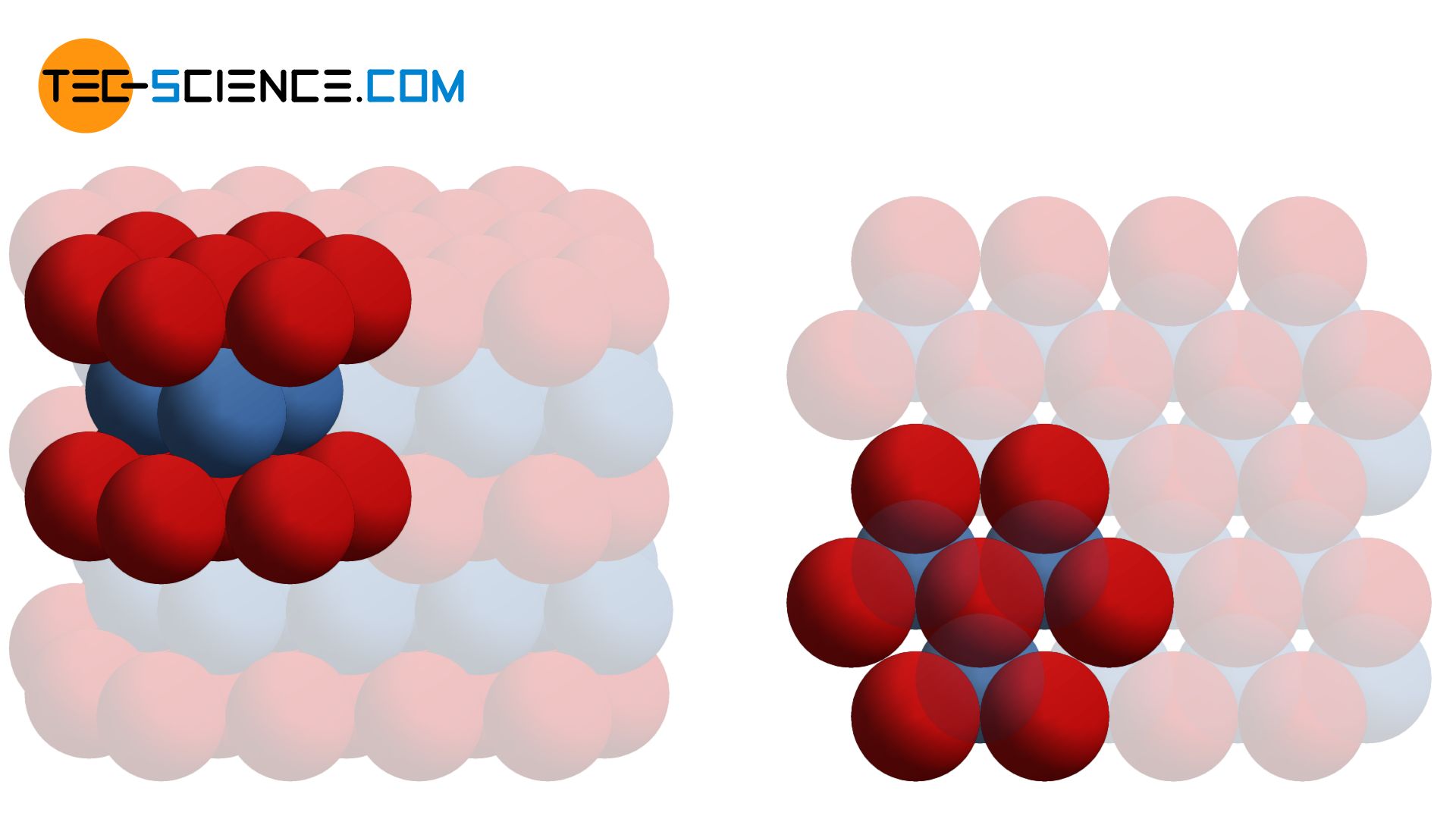
Im hexagonale Gitter sitzen die Atome einer Gitterebene maximal dicht gepackt beieinander. Ein einzelnes Atom in dieser Gitterebene A (rot dargestellt) wird dabei stets von insgesamt sechs benachbarten Atomen berührt. Die darüber liegende Atomebene B (blau dargestellt) ist im Prinzip identisch aufgebaut. Sie liegt jedoch gerade so verschoben, dass die Atome dieser Ebene exakt in die Vertiefungen der darunter befindlichen Ebene passen. Ein Atom der oberen Gitterebene sitzt somit in der Lücke, die von drei Atomen der unteren Schicht gebildet wird. Diese Schichtfolge AB (auch Stapelfolge genannt) wiederholt sich nun permanent (ABAB…).
Als Stapelfolge bezeichnet man die Reihenfolge der sich permanent wiederholenden Atomschichten!
Die Metalle Titan, Kobalt, Zinkt und Magnesium kommen typischerweise in einer solchen hexagonalen Gitterstruktur mit maximaler Packungsdichte vor. Ein Atom im hexagonal-dichtestgepackten Gitter ist von insgesamt 12 direkten Nachbaratomen umgeben. Die Koordinationszahl in diesem Gittertyp beträgt folglich 12.
Die Elementarzelle lässt sich für eine hexagonal-dichtestgepackte Atomanordnung auf eine sechseckige („hexa“) Grundfläche reduzieren. In der Mitte der Elementarzelle befinden sich drei weitere Atome, die in den sich ergebenden Atomlücken der Grund- bzw. Deckfläche sitzen. Da die einzelnen Atomebenen aus denen sich das Gitter aufbaut, maximal gepackt sind, spricht man auch von dichtestgepackte Ebenen. Folglich wird das Gitter auch als hexagonal dichtestgepacktes Gitter (hdp) bezeichnet.
Im hexagonal dichtesgepackten Gitter (hdp) bilden zwei Atomschichten mit einer sechseckigen Grundfläche die Form der Elementarzelle. In der Mitte der Grundflächen befindet sich jeweils ein weiteres Atom, sowie insgesamt drei weitere Atome in der Mitte der Elementarzelle!

Die Packungsdichte im hdp-Gitter entspricht der maximal möglichen Packungsdichte von 74 %. Diese maximale Packungsdichte gilt ganz allgemein für beliebige kugelförmige Körper.
Für kugelförmige Körper ergibt sich eine maximale Packungsdichte von 74 %!
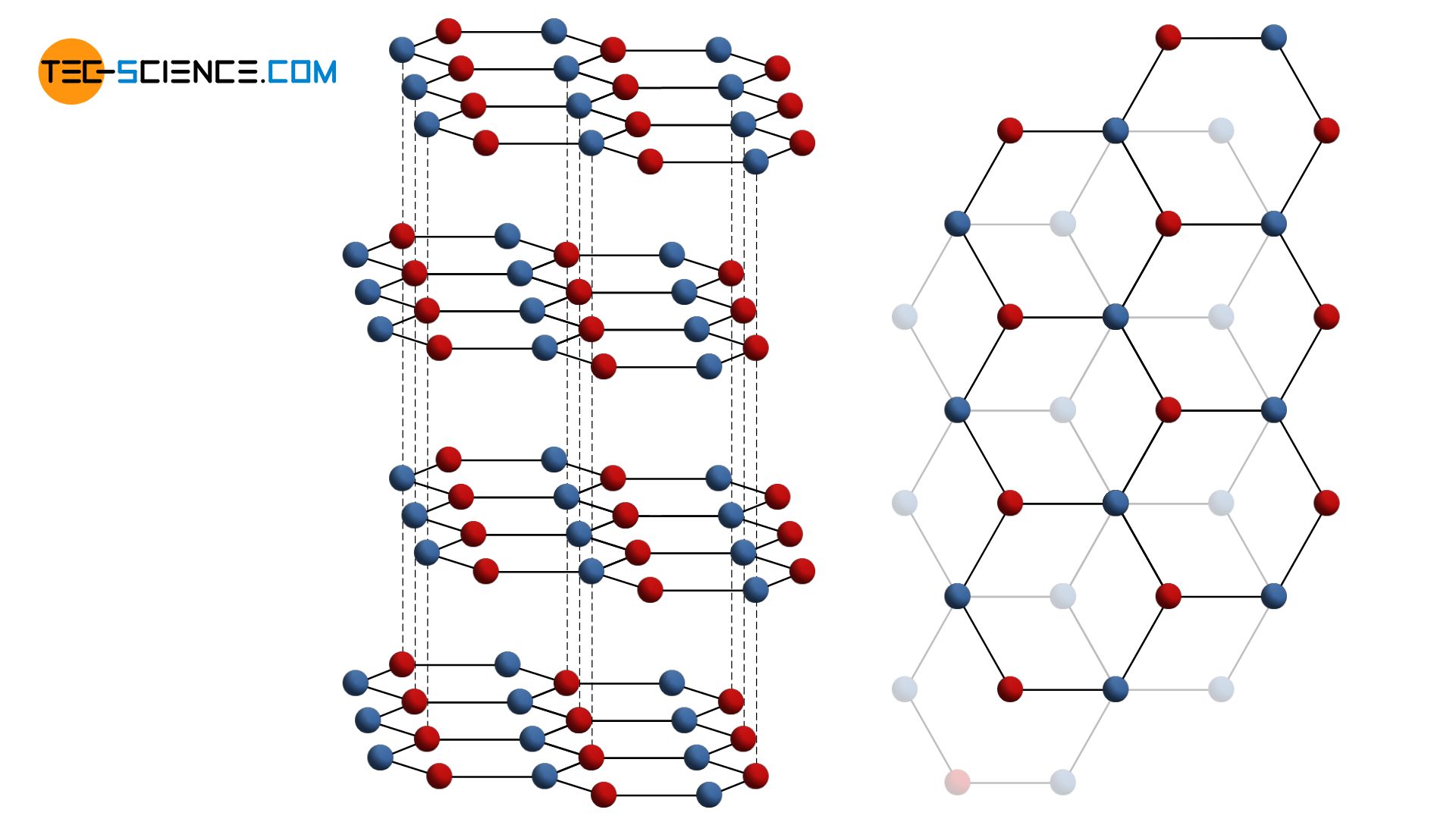
Der Zusatz „dichtest gepackt“ in der Bezeichnung des hexagonalen Gitters impliziert bereits, dass es auch noch andere hexagonale Gitterstrukturen gibt. So besitzt bspw. Graphit ebenfalls eine hexagonale Gitterstruktur (hex), diese ist jedoch nicht dichtest gepackt wie im hdp-Gitter. Während in einer Ebene des hdp-Gitters ein Atom unmittelbar von 6 weiteren Atomen umgeben ist, sind es im hex-Gitter des Graphits nur drei umgebende Atome. Die einzelnen Atomschichten sind dabei versetzt angeordnet und können relativ leicht gegeneinander verschoben werden. Die verschobenen Atomschichten lassen sich hierdurch relativ einfach ablösen. Dieser Vorgang läuft zum Beispiel beim Zeichnen mit einem Bleistift ab, wenn mit der Graphitmine über ein Blatt Papier gefahren wird. Die Graphitschichten der Mine lösen sich ab und bleiben in der Struktur des Papiers haften.
Kubisch-flächenzentriertes Gitter
Das kubisch-flächenzentrierte Gitter (kfz) besitzt wie auch das hexagonal-dichtestgepackte Gitter maximal gepackte Atomebenen. Die Stapelfolge der Ebenen ist jedoch eine andere. Die zweite Ebene ist zunächst noch so gestapelt wie im hdp-Gitter und sitzt in den Lücken der darunter liegenden Schicht. Im Gegensatz zum hdp-Gitter sitzt die dritte Ebene nun allerdings in den „freien“ Lücken. Entsprechend ergibt sich als Schichtfolge der dichtest gepackten Ebenen die Reihe ABCABC…
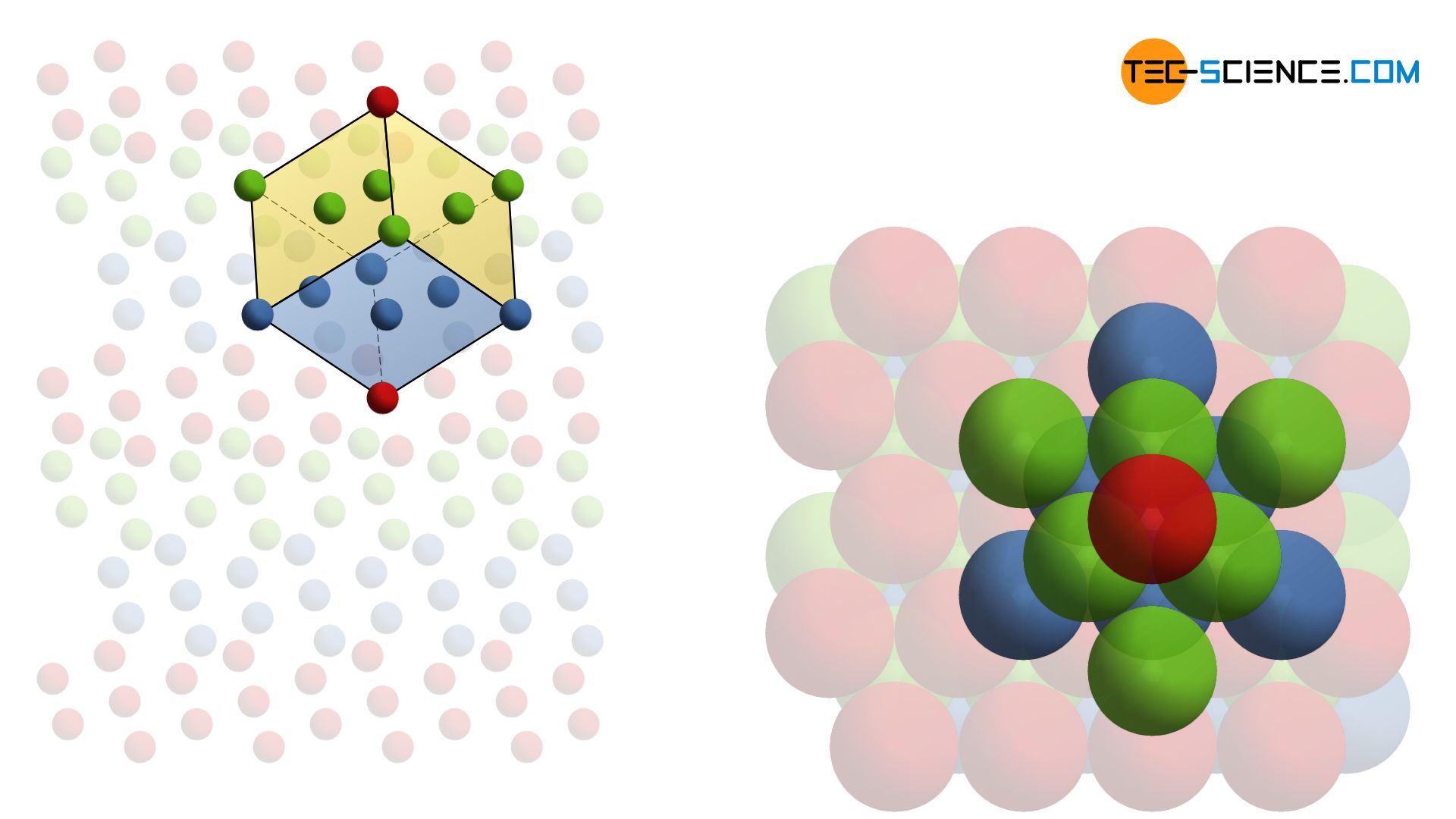
Typische Metalle mit einer kubisch-flächenzentrierten Struktur sind Aluminium, Blei, Kupfer und Nickel. Wie bereits im hdp-Gitter so besitzt auch ein Atom im kfz-Gitter unmittelbar 12 Nachbaratome. Die Koordinationszahl beträgt somit ebenfalls 12.
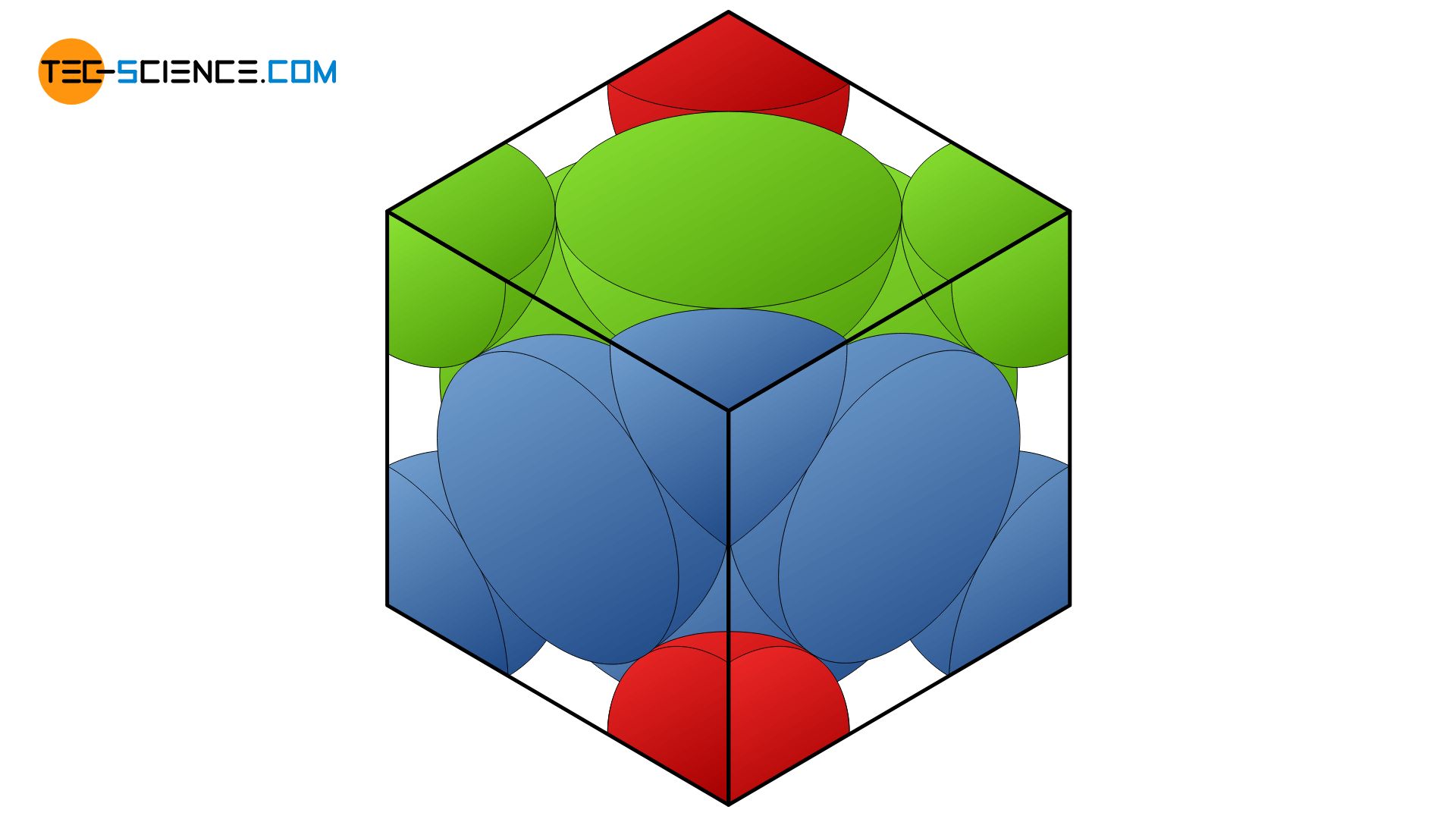
In einem kubisch-flächenzentrierten Gitter ist die Grundform der Elementarzelle nicht etwa hexagonal wie man aufgrund des ähnlichen Aufbaus im Vergleich zum hexagonalen Gitter meinen könnte. Die Elementarzelle hat tatsächlich die Form eines Würfels und zählt deshalb zu den kubischen Kristallsystemen! Bezüglich den horizontal ausgerichteten, dichtestgepackten Ebenen steht die Elementarzelle auf der Würfelspitze. Dabei zeigt sich, dass sich neben den Atomen in den Würfelecken weitere Atome zentriert auf den Würfelflächen befinden. Deshalb bezeichnet man diesen Gittertyp als kubisch-flächenzentriert.
Im kubisch-flächenzentrierten Gitter (kfz) befindet sich neben den Eckatomen jeweils ein weiteres Atom auf den Würfelflächen der kubischen Elementarzelle!
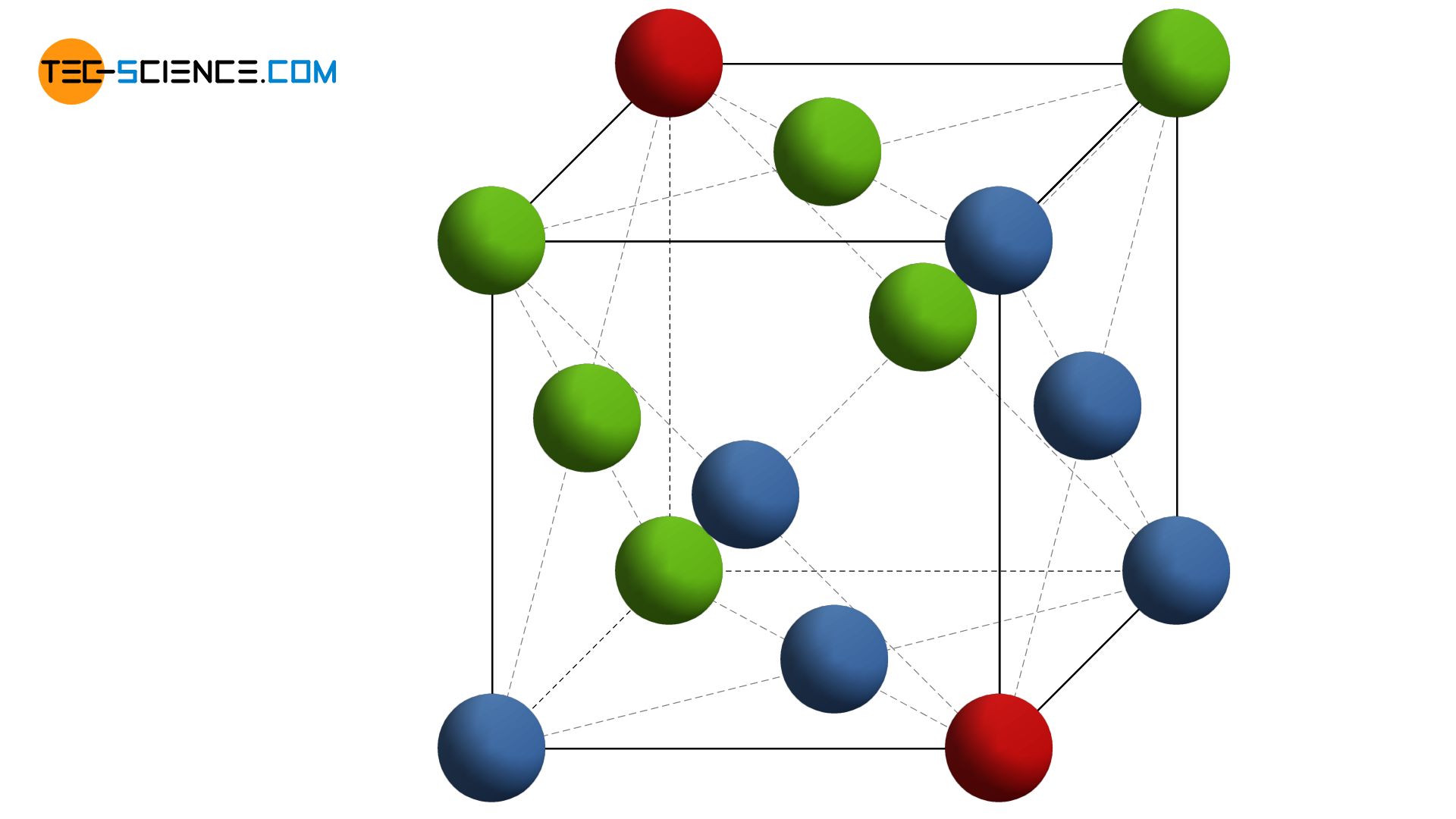
Beachte, dass sich das kfz- und das hdp-Gitter also lediglich in der Stapelfolge der dichtestgepackten Ebenen unterscheiden (ABCABC… bzw. ABAB…)! Die Packungsdichte im kubisch-flächenzentrierten Gitter ist somit identisch mit der maximal möglichen Packungsdichte des hdp-Gitters mit ebenfalls 74 %.
Der zunächst gering erscheinende Unterschied in der Stapelfolge zwischen dem kfz- und dem hdp-Gitter hat allerdings enorme Auswirkungen auf die mechanischen Eigenschaften des Gitters, vor allem auf die Verformbarkeit der Gitterstruktur. Die Ursache hierfür wird im nächsten Beitrag näher erläutert.