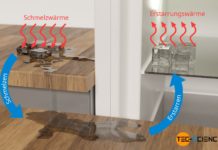
Die zugeführte Verdampfungswärme (Prozessgröße) führt bei einer isobaren Verdampfung zur Änderung der Enthalpie des Stoffes (Zustandsgröße).
Volumenausdehnung beim Verdampfen
Im Artikel Spezifische Verdampfungswärme (latente Wärme) wurde erläutert, dass die Verdampfungswärme für das Aufbrechen der intermolekularen Bindungen erforderlich ist. Tatsächlich müssen beim Verdampfen einer Flüssigkeit aber nicht nur die Bindungsenergien geändert werden. Im Allgemeinen dehnt sich ein Stoff beim Verdampfen auch stark aus. So nimmt gasförmiges Wasser zum Beispiel bei gleichbleibendem Druck von 1 bar ein fast 1700-fach größeres Volumen als flüssiges Wasser ein. Aus einem Liter flüssigem Wasser werden nach dem Verdampfen somit ca. 1700 Liter gasförmiges Wasser („Wasserdampf“)!

Für dieses Ausdehnen entgegen des wirkenden Umgebungsdrucks bzw. für das Hineinschieben des gasförmigen Wasservolumens in die Umgebung ist ebenfalls Energie notwendig. Auch diese aufzubringende Energie wird in Form von Wärme zugeführt und wird in der Verdampfungswärme bereits berücksichtigt! In den meisten Fällen findet ein Verdampfungsvorgang in einem offenen System statt. Die verdampfende Flüssigkeit kann sich somit bei konstantem Umgebungsdruck frei ausdehnen. Man spricht auch von einer isobaren Verdampfung. In diesem Fall lässt sich die für die Volumenänderung aufzuwendende Energie W aus dem Produkt von Druck p und Volumenänderung ΔV ermitteln:
\begin{align}
&\boxed{W = p \cdot \Delta V} \\[5px]
\end{align}
Dieser energetische Umsatz wird aufgrund der damit verbundenen Volumenänderung auch als Volumenänderungsarbeit oder Verschiebearbeit bezeichnet (Hineinschieben des erzeugten Gasvolumens während der Verdampfung in die Umgebung). Beachte jedoch, dass diese aufzuwendenden Energie nicht in Form von mechanischer Arbeit zugeführt wird, sondern ebenfalls durch Wärme.
Man kann sich den Energiebetrag zur Erzeugung des Gasvolumens wie das Ausdehnen eines Luftballons vorstellen. Für das Aufblasen des Luftballons ist Energie nötigt. Diese entspricht im übertragenen Sinne dem Erzeugen des Gasvolumens entgegen dem herrschenden Umgebungsdruck.
Verdampfungsenthalpie
Die Verdampfungswärme kann folglich aufgeteilt werden in einen Anteil, der die Änderung der inneren Energie ΔU in Form geänderter Bindungsenergie bewirkt, und in einen Anteil der die Volumenänderung zur Folge hat.
\begin{align}
\label{h}
&\boxed{Q_\text{V} = \Delta U + p \cdot \Delta V }:= \Delta H_\text{V} ~~~\text{Verdampfungsenthalpie} \\[5px]
\end{align}
Die Summe aus innerer Energie und dem Produkt aus Druck und Volumen wir din der Thermodynamik auch als Enthalpie bezeichnet. Gleichung (\ref{h}) gibt somit die Änderung der Enthalpie des Stoffes durch die isobare Zufuhr der Verdampfungswärme wieder. Die Verdampfungswärme wird deshalb auch als Verdampfungsenthalpie bezeichnet.
Bei einer isobaren Verdampfung kommt die zugeführte Verdampfungswärme vollständig der Änderung der Enthalpie zugute und wird deshalb auch als Verdampfungsenthalpie bezeichnet!
Beachte, dass die Verdampfungswärme und die Verdampfungsenthalpie zwar im Wert identisch sind, jedoch unterschiedliche thermodynamische Bedeutungen haben! Die Enthalpie ist eine Zustandsgröße, die den energetischen Zustand eines Stoffes anhand der inneren Energie und des Drucks bzw. Volumens beschreibt (alle drei Größen sind Zustandsgrößen!). Die Wärme ist hingegen eine Prozessgröße und beschreibt lediglich den Prozess der Energieübertragung in ein System hinein bzw. von einem System heraus. Die über die Systemgrenze hinweg zugeführte Verdampfungswärme ist sozusagen die Ursache für die Änderung der Enthalpie des Systems. Die Verdampfungswärme ist folglich die Ursache und die Enthalpieänderung die hieraus resultierende Wirkung.
Verdampfungsenthalpie am Beispiel von Wasser
Für Wasser soll die Verschiebearbeit während der Verdampfung im Folgenden ermittelt werden. Zunächst nimmt 1 Kilogramm flüssiges Wasser bei einem Druck von 1 bar ein Volumen von rund 1 Liter ein. Nach dem vollständigen Verdampfen ist das Volumen auf rund 1692 Liter angestiegen (dieser Wert kann mit Hilfe der Van-der-Waals-Gleichung ermittelt werden). Die Volumenänderung nach dem Verdampfen beträgt somit ΔV = 1691 Liter. Für diese Volumenänderung ist folglich eine Energie von rund 169 kJ erforderlich:
\begin{align}
&W = p \cdot \Delta V = 1 \cdot 10^5 \tfrac{\text{N}}{\text{m²}} \cdot 1,691 \text{ m³} \approx 169 \text{ kJ} \\[5px]
\end{align}
Die insgesamt zuzuführende Verdampfungswärme für 1 Kilogramm Wasser beträgt gemäß Literatur 2257 kJ. Somit entfallen bei einem Umgebungsdruck von 1 bar folglich rund 7,5 % der insgesamt zugeführten Verdampfungswärme auf die Energie, die zur Vergrößerung des Volumens aufzuwenden sind. Die restlichen 92,5 % der Verdampfungswärme werden dann tatsächlich für die Änderung der Bindungsenergie (Änderung der inneren Energie) genutzt.