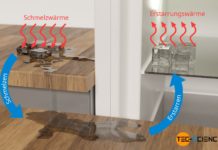
Als spezifische Kondensationswärme bezeichnet man die zur Kondensation eines Gases abzuführende Wärmeenergie pro Kilogramm des Stoffes!
Verdampfung und Kondensation
Im Artikel zur Spezifischen Verdampfungswärme wurde ausführlich erläutert, dass beim Verdampfen einer Flüssigkeit Energie zum Aufbrechen der Bindungen nötig, damit der Stoff in den gasförmigen Zustand überführt werden kann. Diese Energie wird dem Stoff in Form von Wärme zugeführt und wird Verdampfungswärme genannt. Dabei bleibt bei Reinstoffen die Temperatur während der Verdampfung konstant.

Soll der gasförmige Stoff wieder verflüssigt werden, dann muss diesem die zuvor zugeführte Wärme wieder entzogen, damit sich die Moleküle wieder aneinander binden können. Die während der Kondensation des Gases zu entziehende Wärme wird in diesem Fall Kondensationswärme genannt. Auch während des Abführens der Kondensationswärme bleibt die Temperatur dabei konstant. Sie sinkt erst wieder, wenn der gasförmige Stoff vollständig kondensiert ist. Der Temperaturpunkt, bei dem ein Stoff kondensiert, entspricht dem Siedepunkt des Stoffes (Kondensationspunkt).
Eine detailliertere Erklärung für die Notwendigkeit der Wärmeabfuhr während der Kondensation und der Grund weshalb dabei die Temperatur konstant bleibt findet sich im Artikel Warum bleibt die Temperatur bei einer Änderung des Aggregatzustandes konstant? wieder.
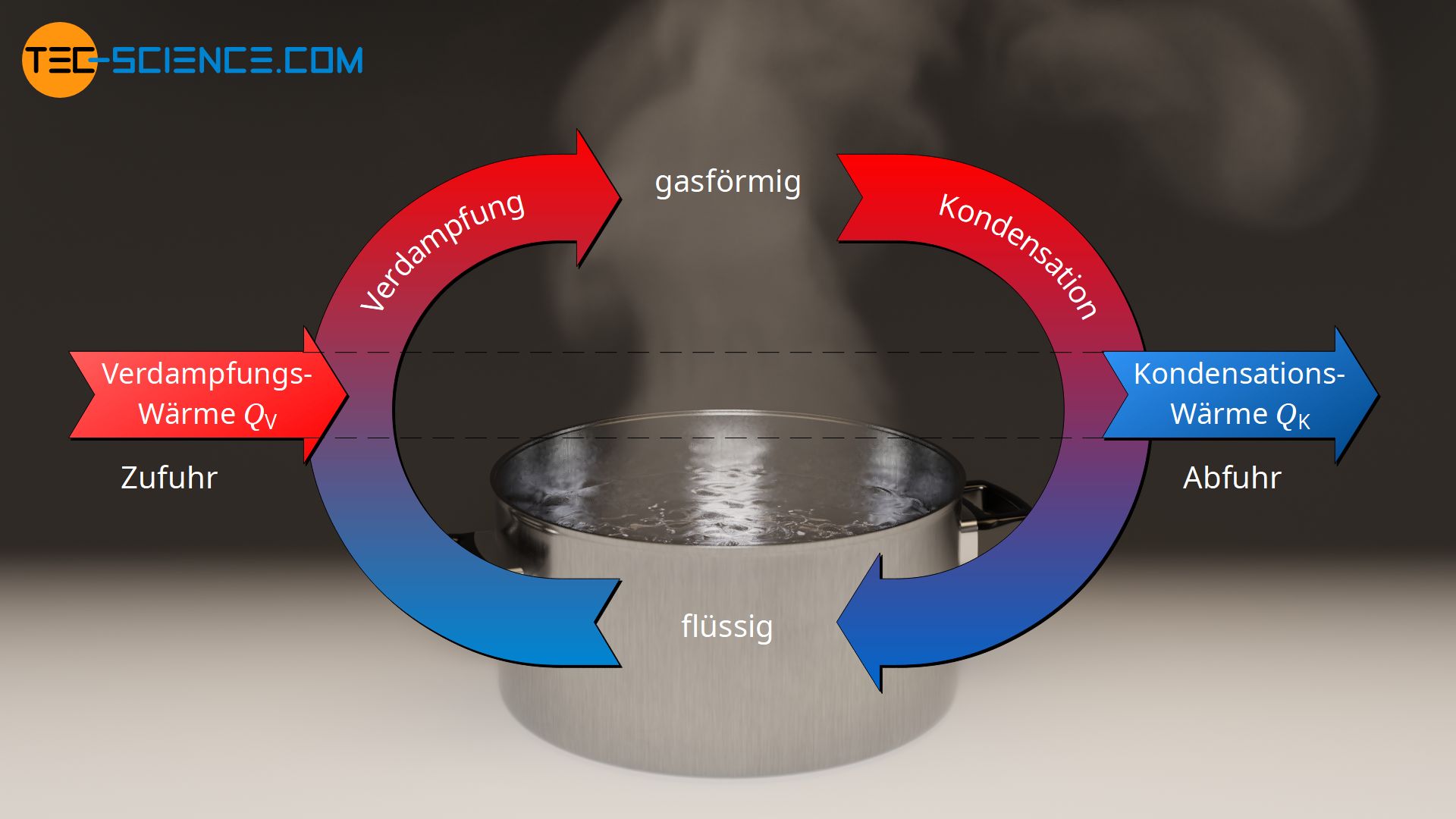
Spezifische Verdampfungswärme und Kondensationswärme
Aufgrund der Energieerhaltung entspricht der Wärmebetrag, der zu Verdampfung eines Stoffes zugeführt wurde (Verdampfungswärme), jener Wärmemenge, die bei der Kondensation wieder abgeführt werden muss (Kondensationswärme). Aus diesem Grund ist auch die spezifische Kondensationswärme qK, als Verhältnis von Kondensationswärme QK und kondensierender Masse mK, genauso groß wie die spezifische Verdampfungswärme qV.
qK=QKmK mit qK=qV
Die spezifische Kondensationswärme ist stoffabhängig und indirekt vom Druck, da durch den Druck der Siedepunkt bzw. Kondensationspunkt beeinflusst wird. Im Artikel Spezifische Verdampfungswärme (latente Wärme) sind für ausgewählte Stoffe die spezifischen Verdampfungswärmen bzw. Kondensationswärmen aufgeführt. Anhand dieser Werte kann die abzuführende Kondensationswärme QK eines Gases in Abhängigkeit der zu kondensierenden Masse mK wie folgt ermittelt werden:
QK=mK⋅qK
Auch man im Falle der Kondensationswärme spricht man wieder von einer latenten Wärme, da sich die abzuführende Wärme beim Kondensieren nicht direkt in einer Temperaturänderung niederschlägt (vom Lateinischen latere, was so viel bedeutet wie „verborgen sein“ oder „sich verstecken„). Im Falle von Wasser ist die beim Kondensieren abzuführende latente Wärme mit 2257 kJ pro Kilogram mehr als fünf Mal so groß wie jene Wärmemenge, die für die Erwärmung des Wassers von 0 °C auf 100 °C hatte aufgewendet werden müssen. Dies erklärt zum Beispiel warum Verbrennungen an Wasserdampf gefährlicher sind als an flüssigem Wasser.
Der Prozess der Abfuhr der Kondensationswärme
Während man beim Verdampfen meist eine sehr anschauliche Vorstellung über den Vorgang der Wärmezufuhr hat, tut man sich bei der Wärmeabfuhr beim Kondensieren manchmal etwas schwer. Verdampft man zum Beispiel Wasser in einem Topf, dann findet der Prozess der Wärmezufuhr sozusagen aktiv durch Erwärmung auf einer Herdplatte statt. Kondensiert hingegen das gasförmige Wasser zum Beispiel wieder an einer Glasscheibe, dann scheint dieser Prozess vordergründig nicht aktiv herbeigeführt worden zu sein. Es scheint als würde der Prozess von selbst abzulaufen, ohne dass aktiv Wärme abgeführt hätte werden müssen.
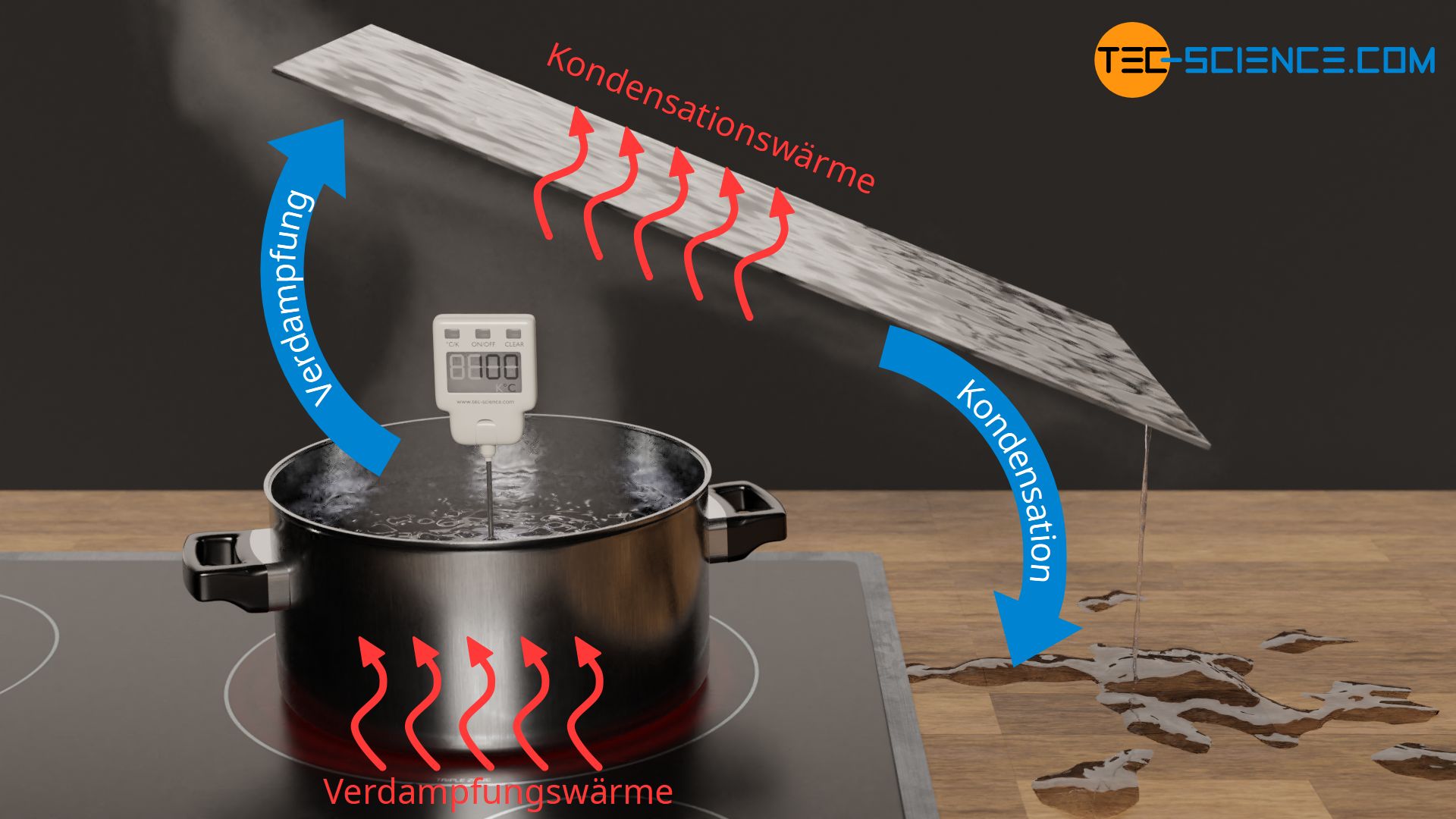
Tatsächlich muss aber auch dabei Wärme abgeführt werden und wird auch. Dies geschieht in diesem Fall durch die kühlere Glasscheibe, welche die Kondensationswärme auf sich vereint und damit an die Umgebung abführt. Auf die analoge Weise wie die heiße Herdplatte aktiv die (Verdampfungs-)Wärme auf das Wasser überträgt, genauso entzieht die kalte Glasplatte wieder aktiv die (Kondensations-)Wärme.
Hätte die Glasscheibe zum Beispiel dieselbe Temperatur von 100 °C wie das gasförmige Wasser, dann würde auch in diesem Fall kein Wasser mehr kondensieren, da kein Wärmestrom vom Wasser auf die Glasscheibe zustände käme. Hätte umgekehrt die Herdplatte dieselbe Temperatur von 100 °C wie das flüssige Wasser, dann käme es auch dabei nicht zu einer Verdampfung, da keine Temperaturdifferenz als Antrieb für den Wärmestrom vorhanden ist.