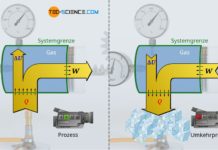
Die Energiezufuhr durch Arbeit während der Kompression eines Gases führt zur Erhöhung des Drucks und der Temperatur.
Während eine Temperaturerhöhung durch Wärmezufuhr direkt aus der Alltagserfahrung heraus nachvollziehbar ist, ist eine Temperaturerhöhung durch eine mechanische Energiezufuhr (Kompressionsvorgang) häufig nicht auf den ersten Blick nachvollziehbar. Vor allem für Gase gibt es für diesen Sachverhalt jedoch eine sehr anschauliche Erklärung. Hierzu soll die Analogie eines Tennisspielers betrachtet werden, auf den gerade ein Tennisball zufliegt. Schlägt der Tennisspieler mit seinem Schläger auf den ankommenden Ball, so wird diesem offensichtlich unter Arbeitsaufwand zusätzlich Bewegungsenergie zugeführt. Der Tennisball fliegt nun mit einer höheren Geschwindigkeit wieder zurück.

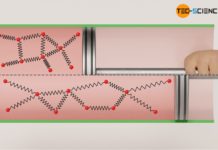
Auf die analoge Weise kann der Kompressionsvorgang eines Gases betrachtet werden. Der Kolben steht dabei für den Tennisschläger und die Gasteilchen für die Tennisbälle. Der den Gasteilchen entgegenkommende Kolben verleiht den Teilchen während des Kompressionsvorganges einen zusätzlichen Impuls und somit zusätzlich kinetische Energie. Die Teilchen werden hierdurch schneller und die Temperatur steigt folglich an! Der Zusammenhang zwischen der mittleren Bewegungsenergie der Teilchen und dem hierdurch hervorgerufenem Druck ist im Artikel Druck und Temperatur näher erläutert.

Die Geschwindigkeit mit der der Kolben das Volumen komprimiert, ist für den Prozess der Temperaturerhöhung relativ unerheblich. Denn wird der Kolben langsam bewegt, so ist die Wucht der Stöße mit einem entgegenkommenden Teilchen zwar geringer, dafür kann der Prozess häufiger stattfinden, wenn das Teilchen nach einer gewissen Zeit wieder auf den bewegten Kolben prallt. Bei einer schnellen Kolbenbewegung, finden hingegen weniger Zusammenstöße mit der Kolbenfläche statt, dafür sind diese allerdings heftiger.
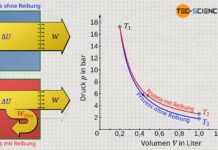
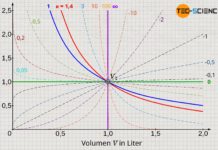
In der Praxis hat die Kompressionsgeschwindigkeit insofern einen Einfluss, da die Temperaturerhöhung bei relativ langsamer Kompression durch ein Wärmestrom über die Zylinderwände wieder etwas kompensiert werden kann. Die Endtemperatur nach der Kompression wird durch die abgehende Wärmeenergie also nicht so hoch sein. Wird hingegen sehr rasch komprimiert, so kann innerhalb der kurzen Zeit kaum Wärme über die Zylinderwände auf die Umgebung übertragen werden (man spricht in diesem Fall auch von einem adiabaten System). Der Temperaturanstieg findet in vollem Maße statt. Die sich einstellende Endtemperatur nach dem Verdichtungsvorgang wird dementsprechend größer sein.
Man kann die Temperaturerhöhung während einer (adiabaten) Kompression mit folgendem Experiment demonstrieren. Ein Zylinder ist mit einem beweglichen Kolben verschlossen. In den Zylinder wird ein Wattebausch gelegt. Drückt man den Kolben schlagartig nach unten, so findet durch den Verdichtungsvorgang ein so starker Temperaturanstieg statt, dass sich die Watte entzündet. Nach diesem Prinzip der sogenannten Selbstzündung arbeiten im Übrigen Dieselmotoren. Anstelle von Watte wird dabei ein Benzin-Luft-Gemisch gezündet.