Als reversible Prozesse werden in der Thermodynamik Zustandsänderungen bezeichnet, die aus energetischer Sicht umkehrbar sind!
Einleitung
Die freie adiabate Expansion eines idealen Gases in einem Vakuum zeigte, dass sich dieser Prozess nicht mit den Isentropengleichungen beschreiben lässt, obwohl diese Gleichungen für ein adiabates System hergleitet wurden. Vielmehr handelt es sich bei dieser Expansion um einen isothermen Prozess, bei dem die Temperatur konstant bleibt. Es stellt sich deshalb die Frage, welche Bedingung einem adiabaten System zugrunde liegen muss, damit die darin ablaufenden thermodynamischen Prozesse tatsächlich mit den isentropen Zustandsgleichungen beschrieben werden können.
Umkehrbarkeit thermodynamischer Prozesse
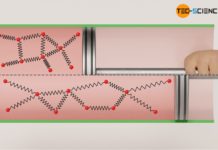
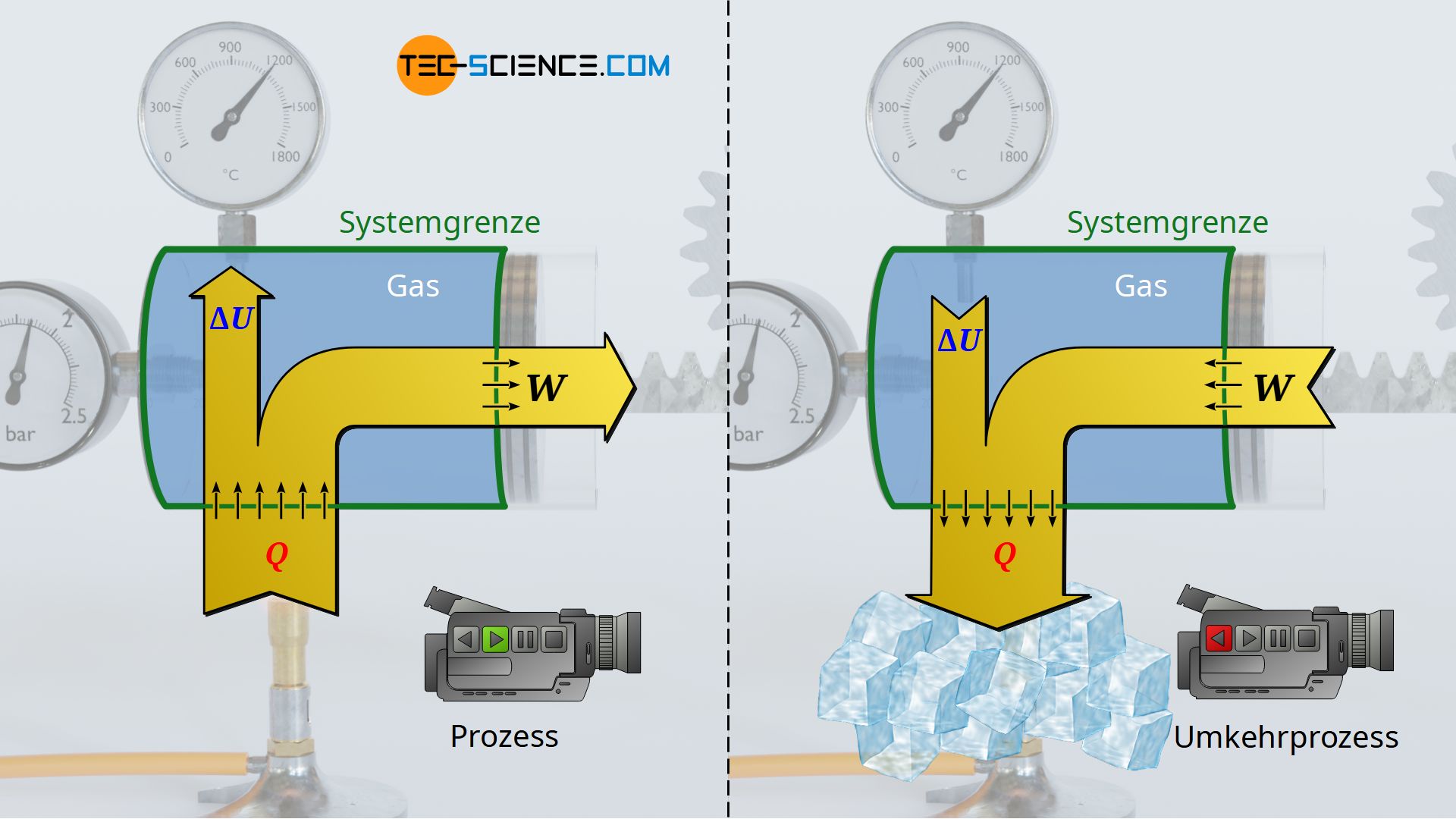
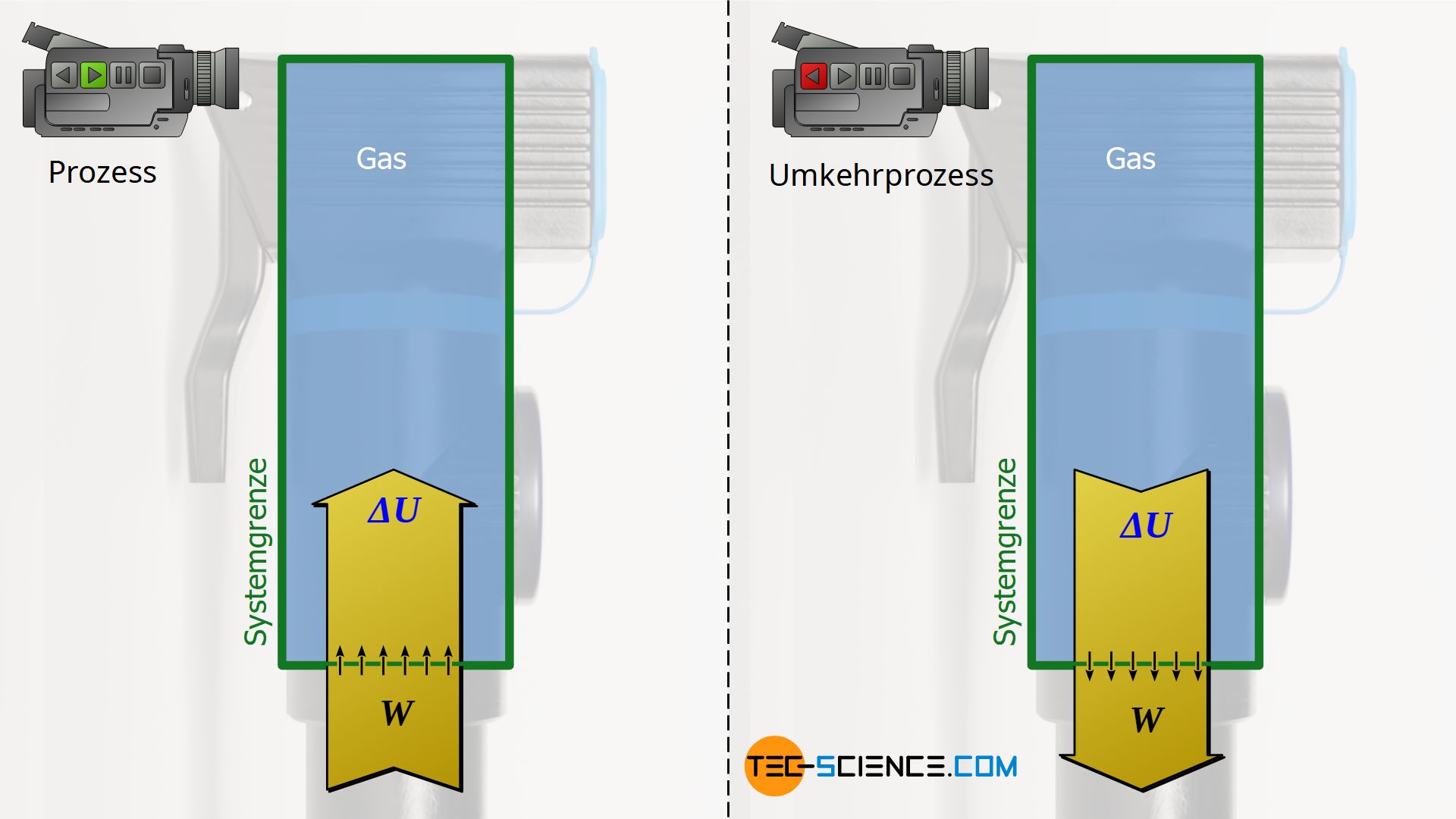
Hierzu betrachten wir ausgewählte thermodynamische Prozesse etwas genauer. Dabei wird man feststellen, dass all diese Prozesse aus energetischer Sicht sowohl in die eine als auch prinzipiell in die andere Richtung ablaufen können. So wurde im Artikel Volumenänderungsarbeit jener thermodynamische Vorgang betrachtet, bei dem ein Gas in einem Zylinder unter Wärmezufuhr expandiert und über eine am Kolben befindliche Zahnstange mit Zahnrad schließlich ein Gewicht anhebt. Aus energetischer Sicht lässt sich dieser Prozess prinzipiell umkehren.

Hierzu kann man sich den ursprünglichen Prozess als mit einer Videokamera aufgenommen vorstellen, die anschließend rückwärts abgespielt wird. In einem solchen umgekehrten Fall senkt sich das Gewicht unter Wärmeabfuhr (Kühlung) wieder. Dabei wird nicht mehr Arbeit vom Gas am Gewicht verrichtet, sondern es wird umgekehrt Arbeit am Gas vom Gewicht verrichtet – das Gas wird sozusagen durch das Gewicht komprimiert. Gleichzeitig sinkt durch die Kühlung die Temperatur und mit ihr die innere Energie. Die Energieflüsse kehren sich bei einem solchen Umkehrvorgang also gerade um, ohne dass man dabei aus der Erfahrung heraus auf einen Widerspruch stoßen würde.
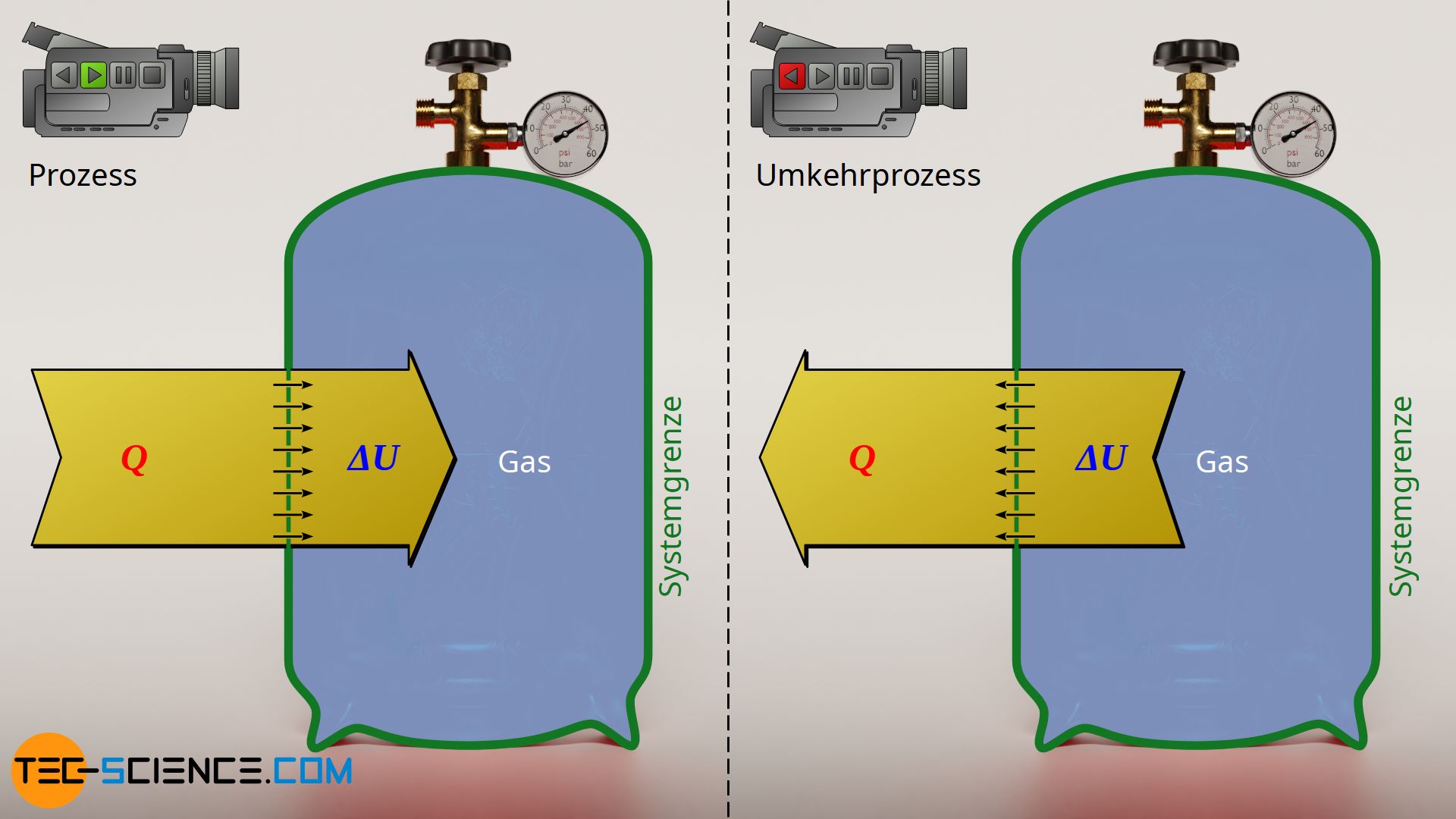
Isochorer Prozess
Auch bei einem isochoren Aufheizprozess einer Gasflasche, lässt sich ein solcher Umkehrprozess finden. Dabei findet aufgrund der zugeführten Wärme eine Erhöhung innere Energie statt, d.h. die Temperatur steigt an. Wird dieser Vorgang energetisch umgekehrt betrachtet, so erhielte man einen isochoren Abkühlprozess. In einem solchen Umkehrfall würde sich die innere Energie durch die abgeführte Wärme erniedrigen und sich die Temperatur folglich erniedrigen.
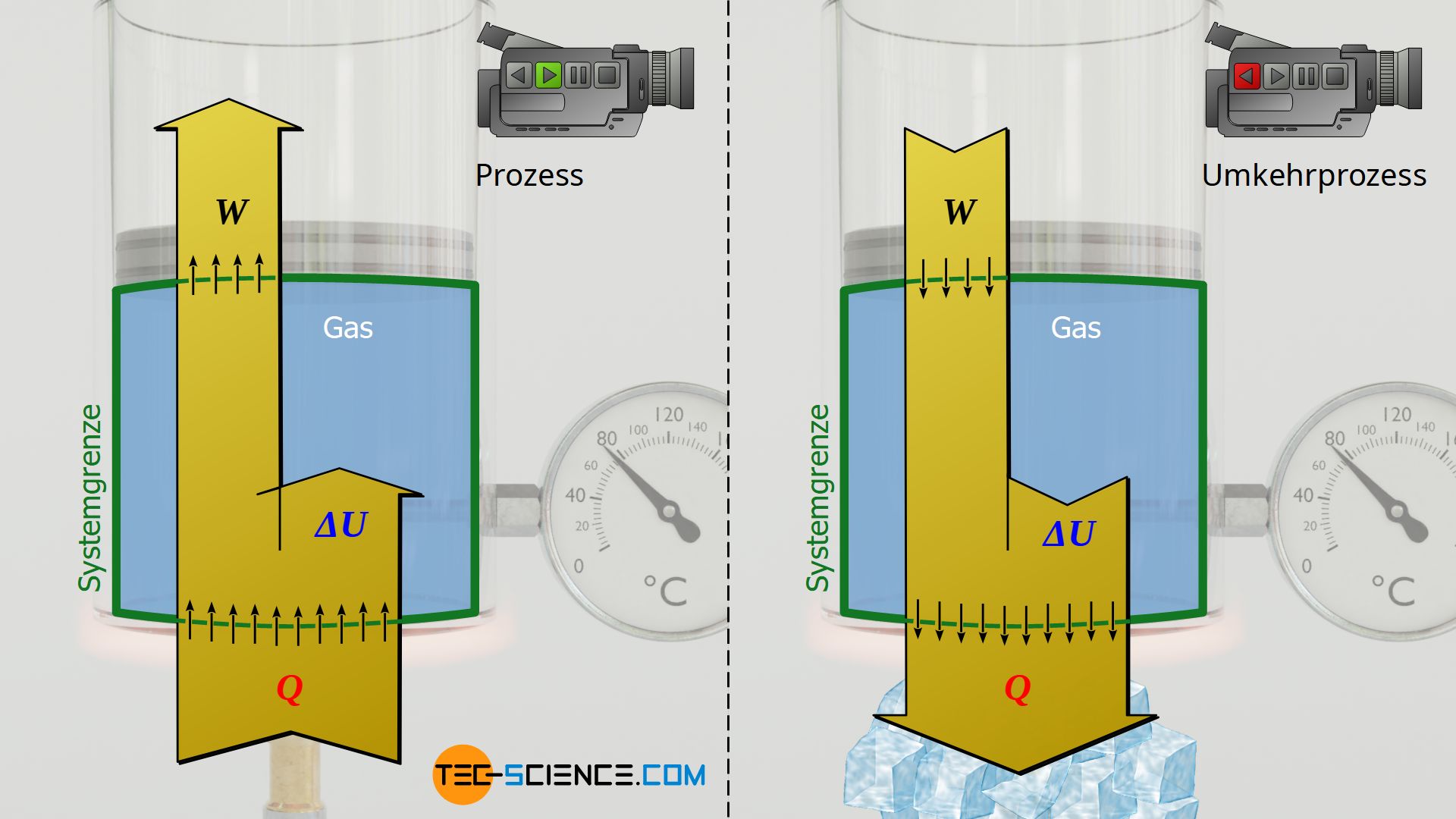
Isobarer Prozess
Auch der im Artikel zum isobaren Prozess erläuterte Prozess, bei dem unter Wärmezufuhr ein Gewicht angehoben wird, lässt sich energetisch umkehren. Dabei verrichtet das Gas zunächst unter Zufuhr von Wärme Arbeit, während sich die innere Energie erhöht und die Temperatur folglich ansteigt. Im umgekehrten Fall erhielte man einen isobaren Abkühlprozess, bei dem das Gas unter Zufuhr von Arbeit komprimiert wird, während gleichzeitig Wärme abgeführt wird. Insgesamt verringert sich dabei die innere Energie und somit auch die Temperatur wieder.
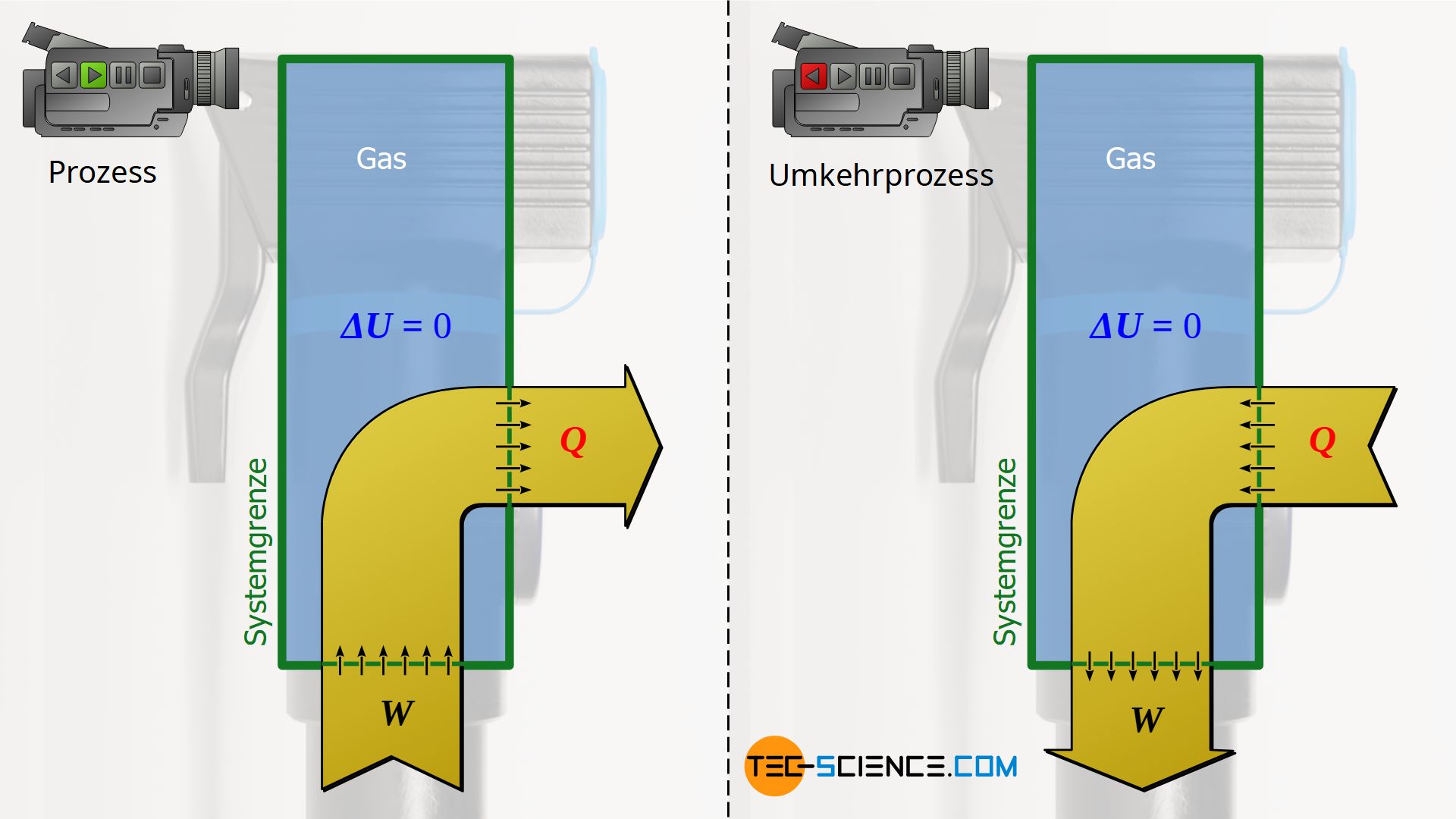
Isothermer Prozess
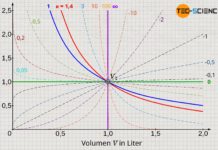
Auch die im Artikel zum isothermen Prozess erläuterte Kompression der Luft in einer Luftpumpe zeigt eine solche energetische Umkehrbarkeit. Wird das Gas in einer Luftpumpe bei verschlossenem Ventil sehr langsam komprimiert, so erhält man durch die gleichzeitig stattfindende Wärmeabfuhr auf die Umgebung eine (nahezu) gleichbleibende Temperatur. Umgekehrt kann das Gas aus diesem komprimierten Zustand auch wieder isotherm expandieren. Hierzu muss die Zustandsänderung wieder sehr langsam erfolgen, sodass die Umgebung dem expandierenden Gas ausreichend Wärme zufuhren kann, um eine Temperaturverringerung während der Expansion zu verhindern.
Isentroper Prozess
Ebenfalls kann die im Artikel zum isentropen Prozess vorgestellte schnelle Kompression der Luft in einer Luftpumpe aus energetischer Sicht umgekehrt werden. Dabei wird ein Gas zunächst unter Aufwendung von Arbeit rasch komprimiert, was zu einer entsprechenden Erhöhung der inneren Energie führt und die Temperatur ansteigen lässt. Im umgekehrten Fall würde dies bedeuten, dass das Gas ausgehend des komprimierten Zustandes sehr rasch wieder expandiert. Bei diesem isentropen Umkehrprozess wird dann Arbeit auf Kosten der inneren Energie nach außen abgegeben und die Temperatur sinkt folglich.
Reversibilität
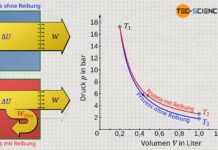
Die in den Abschnitten zuvor betrachteten Prozesse machen deutlich, dass diese aus energetischer Sicht alle umkehrbar sind. In der Fachsprache bezeichnet man solche (energetisch) umkehrbaren Vorgänge als reversible Prozesse (engl. reverse = umkehren). Die Reversibilität von Vorgängen setzt unter anderem die Annahme voraus, dass die Zustandsänderungen allesamt reibungsfrei ablaufen bzw. es sich nicht um dissipative Prozesse handelt (z.B. wenn ein Kolben in einem Zylinder gleitet).
In der Thermodynamik sind reversible Prozesse Vorgänge, die aus energetischer Sicht umkehrbar sind, ohne dabei die Alltagserfahrung zu verletzen!
Darüber hinaus muss es sich bei den Gaszuständen stets um Gleichgewichtszustände handeln, sodass es nicht zu einem Temperaturunterschied innerhalb des Gases kommt. Sowohl die Annahme der Reibungsfreiheit als auch die Annahme des stets vorhandenen Gleichgewichtszustandes ist natürlich nur idealisiert. Somit existieren reversible Prozesse auch nur in idealisierten Vorstellungen. Diese Idealbedingungen wurden bisher bei allen betrachteten Vorgängen angenommen.
Adiabate Expansion gegen ein Vakuum als nicht-umkehrbarer Prozess
Was die Reversibilität angeht, sieht die Situation bei der adiabaten Expansion gegen ein Vakuum jedoch anders aus. Dieser thermodynamische Prozess ist aus der Erfahrung heraus nicht umkehrbar. So expandierte das Gas bei gleichbleibender Temperatur ohne Zu- oder Abfuhr von Arbeit bzw. Wärme. Umgekehrt müsste dies bedeuten, dass das Gas wieder ohne Arbeits- und Wärmeumsatz von selbst komprimiert. Das Gas müsste sich praktisch ohne äußeres Zutun bei gleichbleibender Temperatur wieder von selbst wieder zusammenziehen.

Dies widerspricht jeglicher Erfahrung, denn um ein Gas in einem Zylinder zu komprimieren, muss von außen Arbeit aufgebracht werden – ein Gas wird dies nicht von selbst tun. Dabei würde die Temperatur dann auch nicht mehr konstant bleiben, sondern sie würde sich aufgrund der zugeführten Arbeit erhöhen. Eine adiabate Expansion gegen ein Vakuum ist aus energetischer Sicht folglich ein nicht-umkehrbarer Prozess. Solche nicht umkehrbaren Vorgänge werden auch als irreversible Prozesse bezeichnet.
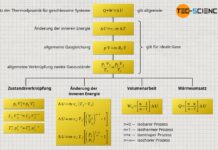
Grundsätzlich gelten alle in den entsprechenden Artikeln vorgestellten Gleichungen – insbesondere die des isochoren, isobaren, isothermen und isentropen Prozesses – nur für reversible Prozesse, also für Zustandsänderungen die prinzipiell umkehrbar sind! Dies erklärt nun auch weshalb die Gleichungen des isentropen Prozesses im Expansionsbeispiel gegen das Vakuum nicht angewendet werden können. So handelt es sich zwar um ein adiabates System, der Prozess selbst ist aber irreversibel! Die Gleichungen des isentropen Prozesses dürfen nur verwendet werden, wenn es sich um eine reversible Zustandsänderung eines adiabaten Systems handelt. Somit lässt sich eine isentrope Zustandsänderung wie folgt definieren:
Als isentroper Prozess bezeichnet man eine reversible Zustandsänderung eines adiabaten Systems!
Die Umkehrbarkeit von Vorgängen wird in der Thermodynamik durch den Entropiebegriff beschrieben. Für die reversible Zustandsänderung des adiabaten Systems bleibt die Entropie konstant, wovon sich der Begriff isentroper Prozess ableiten lässt (=“ gleichbleibende Entropie“).