Das Bohr-Sommerfeld Modell ist eine Erweiterung des Schalenmodells von Bohr. Hierdurch kann die Besetzungsreihenfolge der Schalen mit Elektronen erklärt werden (Elektronenkonfiguration).
Die Schwächen des Bohr’schen Atommodells konnten durch den Physiker Arnold Sommerfeld teilweise beseitigt werden. So führte Sommerfeld im Prinzip neben den bereits eingeführten Schalen auch sogenannte Unterschalen ein (auch Orbitale genannt). Man spricht in diesem Zusammenhang auch von der sogenannten Sommerfeld-Erweiterung, die das Bohr’sche Atommodell erfuhr.
Mit Einführung der Unterschalen konnte mit Ausnahmen einiger Atome schließlich die Besetzungsreihenfolge der Schalen mit Elektronen erklärt werden. Diese Elektronenverteilung im Atom wird auch als Elektronenkonfiguration bezeichnet. Sie soll im Folgenden näher erläutert werden.
Dabei stellt man sich die durch Bohr eingeführten Hauptschalen in Unterschalen gedacht vor. Wie viele Unterschalen eine Hauptschale besitzt, hängt von der Stellung der Schale ab. Dabei gibt die Hauptschalennummer gerade die Anzahl der Unterschalen an. In der oberen Abbildung oben sind nicht alle Unterschalen der höheren Hauptschalen abgebildet, da diese in der Regel keine Relevanz besitzen. Die Unterschalen werden nicht mit Zahlen sondern jeweils mit Kleinbuchstaben (s, p, d und f) bezeichnet.
Als Eselsbrücke kann man sich die Partei „SPD“ und das Dateiformal „PDF“ vorstellen, die mit ihren Buchstaben die Reihenfolge der Unterschalen wiedergeben. Eine g-Unterschale existiert lediglich für theoretische Elemente ab Ordnungszahlen größer 121 (auch Superactinoide genannt), weshalb dieses Orbital für die Praxis keine Bedeutung hat.
- 1. Hauptschale (K): 1 Unterschale (s), identisch mit der Hauptschale
- 2. Hauptschale (L): 2 Unterschalen (s, p)
- 3. Hauptschale (M): 3 Unterschalen (s, p, d)
- 4. Hauptschale (N): 4 Unterschalen (s, p, d, f)
Die Schalenbezeichnung 3p meint beispielsweise die Unterschale p („2. Unterschale“) der dritten Hauptschale und die Bezeichnung 4s die Unterschale s („1. Unterschale“) der vierten Hauptschale. Die Schalenbezeichnung 2d gibt es hingegen nicht, da die zweite Hauptschale lediglich eine s- und eine p-Unterschale besitzt! Auf den Unterschalen hat auch jeweils nur eine bestimmte Anzahl an Elektronen Platz:
- s-Unterschale: 2 Elektronen
- p-Unterschale: 6 Elektronen
- d-Unterschale: 10 Elektronen
- f-Unterschale: 14 Elektronen
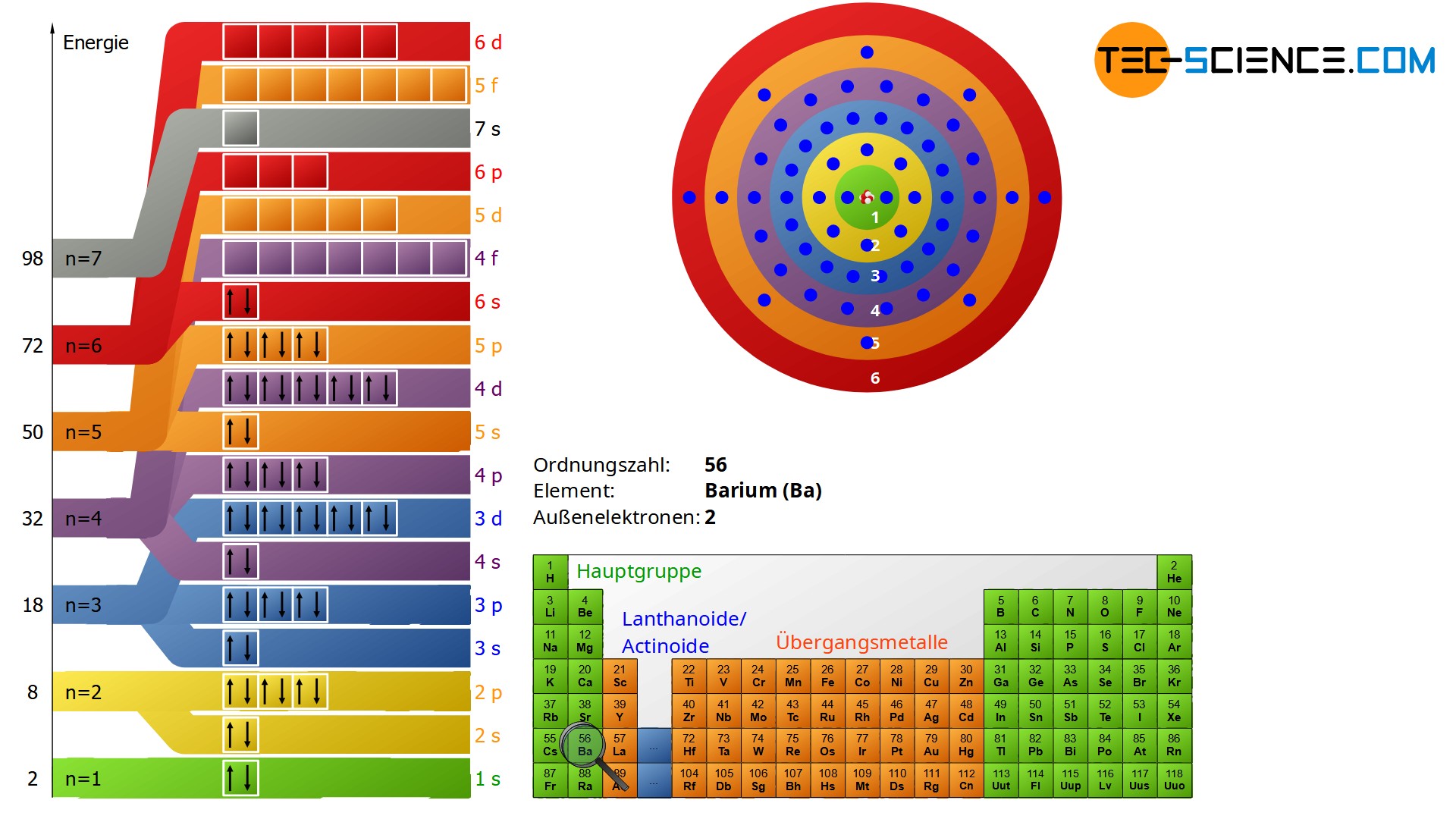
Dabei kann eine Unterschale einer niedrigeren Hauptschalennummer durchaus ein höheres Energieniveau aufweisen als die Unterschale einer höheren Schalennummer (Sommerfeld erklärte dies mit elliptischen Bahnen der Elektronen anstelle von einfachen Kreisbahnen nach Bohr)! So besitzt bspw. die Unterschale 3d einen höheren Energiewert als die unterschale 4s! Die graphische Darstellung durch Schalen mit ihren Unterteilungen in Unterschalen ist deshalb so einfach auch nicht mehr möglich. Vielmehr wird die grafische Darstellung anschaulicher durch das Orbitalmodell beschrieben, auf welches an dieser Stelle nicht weiter eingegangen werden soll. Die genaue energetische Verteilung der Unterschalen im Schalenmodell ist in der Abbildung oben gezeigt. Hierin sind die Unterschalen in weiß umrandete Blöcke aufgeteilt, die jeweils Platz für insgesamt zwei Elektronen bieten.
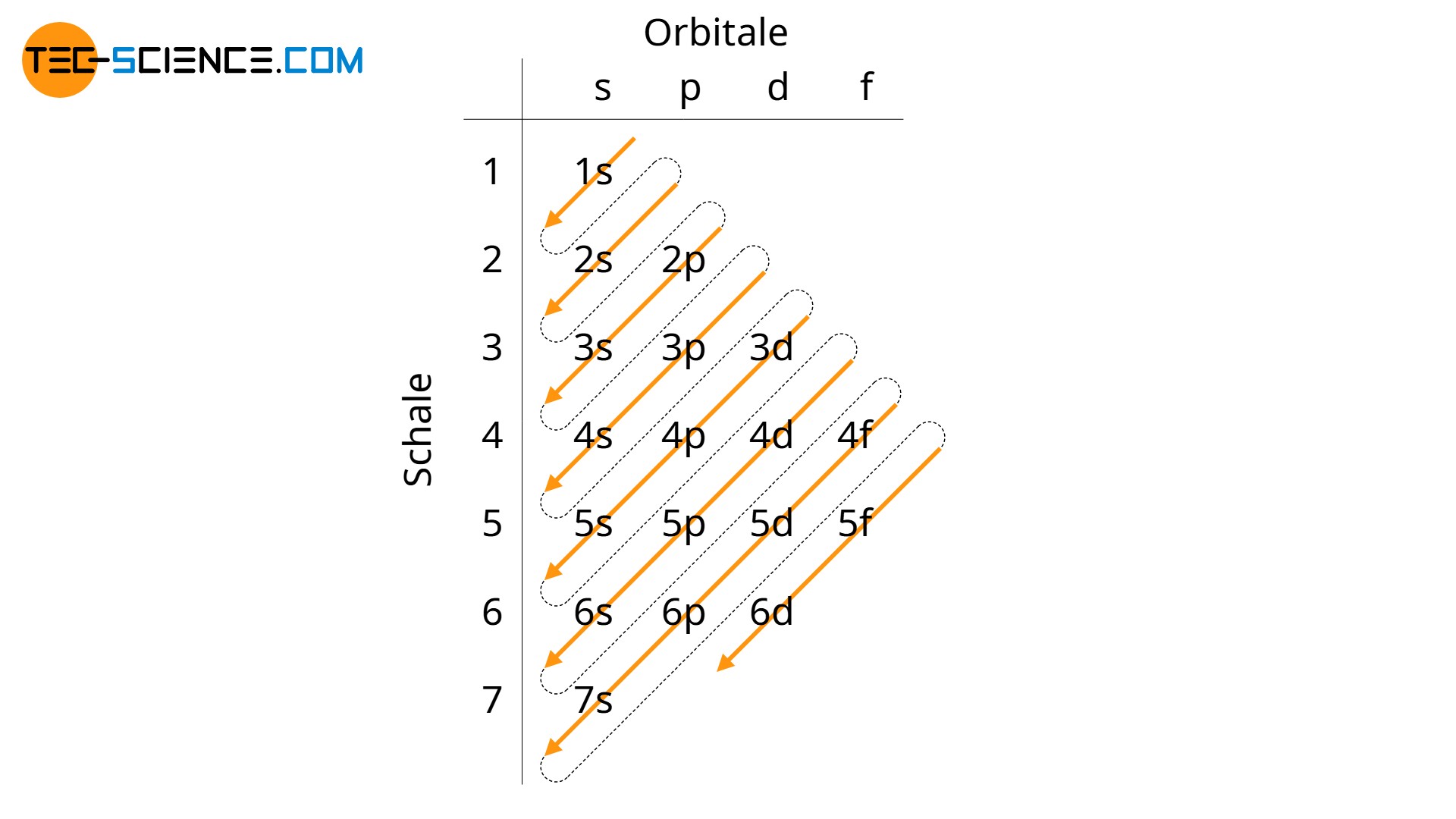
Um sich die energetische Reihenfolge der Orbitale besser merken zu können, kann man sich zunächst eine Tabelle anlegen. Darin entspricht die Zeilennummerierung der Hauptschalennummer und die Spaltennummerierung der Unterschale. Somit ist für jedes Feld die Unterschale mit zugehöriger Hauptschale eindeutig festgelegt. Die energetische Reihenfolge der Orbitale erhält man nun, indem man die Tabelle jeweils zeilenweise schräg von rechts oben nach links unten durchgeht.
Die Animation unten zeigt die Elektronenbesetzung der Schalen mit größer werdender Ordnungszahl der Atome. Beachte, dass die Elektronenzahl im selben Maße wie die Protonenzahl zunimmt und somit von Element zu Element um eins ansteigt. Die zu einer Hauptschale gehörenden Unterschalen sind dabei alle in einer einheitlichen Farbe markiert. Ebenfalls dargestellt sind die Außenelektronen (Valenzelektronen) auf der äußersten Hauptschale (Valenzschale), da diese für das chemische Verhalten eines Stoffes maßgebend sind. Diese Animation erklärt auch die Ordnung der chemischen Elemente im Periodensystem.
Die Besetzung der Schalen mit Elektronen erfolgt grundsätzlich immer ausgehend des energieärmsten Zustandes, erst anschließend werden höhere Energieniveaus besetzt. Dabei wird jeder Block einer Unterschale zunächst mit nur einem Elektron gefüllt. Dies wird durch einen aufsteigenden Pfeil symbolisiert. Sind alle Blöcke einer Unterschale einfach gefüllt, dann erfolgt der zweite Durchlauf. Dabei wird die Elektronenbesetzung durch einen abwärts gerichteten Pfeil dargestellt. Diese symbolische Unterscheidung ist dem sogenannten Pauli-Verbot der Quantenmechanik geschuldet, nach dem keine zwei identischen Elektronenzustände existieren können. Die unterschiedlichen Pfeilrichtungen tragen diesem Prinzip Rechnung (die Pfeile repräsentieren jeweils eine von insgesamt zwei Spinquantenzahlen).
Bei der Unterschale 3p fällt auf, dass nachdem diese vollständig mit Elektronen befüllt wurde, es energetisch günstiger ist eine vierte Hauptschale anzufangen und mit Elektronen zu befüllen (4s-Schale) anstelle der Unterschale 3d! An diesem Beispiel wird das zuvor Erläuterte deutlich, dass Unterschalen einer geringeren Hauptschalennummer durchaus ein höheres Energieniveau besitzen als Unterschalen einer höheren Hauptschale. Damit kann nun auch die für einen außenstehenden zunächst komisch erscheinende Elektronenbesetzung der Hauptschalen erklärt werden.
Erst nachdem das 4s-Orbital vollständig besetzt ist, wird die dritte Hauptschale mit dem energetisch höher gelegenen 3d-Orbital weiter aufgefüllt. Dieser Sprung macht sich auch im chemischen Verhalten bemerkbar. Er kennzeichnet den Übergang von den sogenannten Hauptgruppenelementen zu den Nebengruppenelementen (auch als Übergangselemente oder Übergangsmetalle bezeichnet). Die Übergangsmetalle zeichnen sich also dadurch aus, dass diese jeweils ein nicht vollständig besetztes d-Orbital besitzen (auch d-Block genannt).
Ein weiterer Sprung um sogar zwei Hauptschalen zeigt sich bei dem Übergang vom Element Barium (Ba) zu Cer (Ce). Nachdem bei Barium das 6s-Orbital vollständig befüllt wurde, ist nun bei Cer zwei Hauptschalen „zurückgesprungen“ worden und das 4f-Orbital wird weiter aufgefüllt (das dazwischenliegende Lanthan stellt eine Ausnahme der Aufbauregel dar). Dieser Übergangssprung leitet eine Untergruppe der Übergangsmetalle ein, die sogenannten Lanthanoiden bzw. Actinoiden (auch f-Block genannt). Bei diesen Metallen wird somit das f-Orbital nach und nach mit Elektronen befüllt. Strenggenommen zählen die Elemente Lanthan und Actinium selbst nicht zur Gruppe der Lanthanoiden bzw. Actinoiden, obgleich sie aus praktischen Gründen sehr häufig hierzu mitgezählt werden. Deshalb fallen auch diese Elemente in den f-Block.
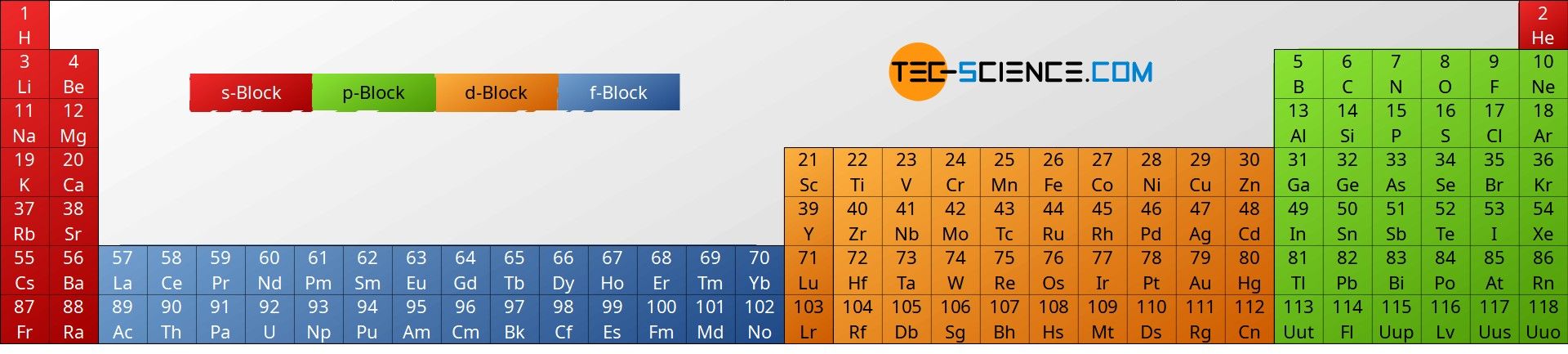
Je nachdem auf welchem Orbital ein Elektron hinzukommt, kann man das Periodensystem in Blöcke aufteilen, die entsprechend mit s, p, d oder f bezeichnet werden.
Von der oben beschriebenen Besetzungsregel gibt es jedoch auch Ausnahmen. Dies trifft bspw. für die Metalle Kupfer und Chrom zu. Dort wechselt ein Elektron von der 4s-Unterschale auf die 3d-Unterschale und bleibt somit nur mit einem Elektron besetzt. Solche Ausnahmen von der regulären Aufbauregel finden sich vor allem bei höheren Ordnungszahlen, da sich die Elektronen mehr und mehr gegenseitig beeinflussen. Zudem kommen relativistische Effekte zum Tragen, die in dieser einfachen Aufbauregel nicht berücksichtigt sind. Die Ausnahmen von der regulären Aufbauregel sind im Video entsprechend angemerkt.